
| 实验原理 | m=cVM |
| 实验仪器 | 托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管 |
| 实验步骤 | (1)计算:溶质Na2SO4固体的质量为28.4g. (2)称量:用托盘天平称取所需Na2SO4固体. (3)溶解:将称好的Na2SO4固体放入烧杯中,用适量蒸馏水溶解. (4)转移、洗涤:将烧杯中的溶液冷却至室温并注入仪器①中,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也都注入仪器①中. (5)定容:将蒸馏水注入仪器至液面离刻度线1~2cm时,改用胶头滴管滴加蒸馏水至液面与刻度线相切. (6)摇匀:盖好瓶塞,反复上下颠倒,然后静置. |
| 思考与探究 | (1)实验步骤(3)、(4)中都要用到玻璃棒,其作用分别是搅拌、引流 (2)某同学在实验步骤(6)后,发现凹液面低于刻度线,该同学所配置溶液是浓度=(填“>”、“=”或“<”)0.4mol/L. |
分析 实验仪器:配制一定物质的量浓度溶液一般步骤为:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等,据此选择需要的仪器,判断缺少的仪器;
实验步骤:(1)依据m=CVM计算需要溶质的质量;
思考与探究:(1)依据溶解过程中为加速固体溶解速率,需要用玻璃棒搅拌,移液操作中用玻璃棒引流解答;
(2)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:实验仪器:配制一定物质的量浓度溶液一般步骤为:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等,用到的仪器有:托盘天平、药匙、烧杯、筒量、玻璃棒、容量瓶、胶头滴管,缺少的仪器为:500mL容量瓶;
故答案为:容量瓶;
实验步骤:(1)配制500mL 0.4mol/L Na2SO4溶液,需要溶质的质量m=0.4mol/L×0.5L×142g/mol=28.4g;
故答案为:28.4;
思考与探究:(1)溶解过程中为加速固体溶解速率,需要用玻璃棒搅拌,移液操作中用玻璃棒引流;
故答案为:引流;
(2)某同学在实验步骤(6)后,发现凹液面低于刻度线,属于正常操作,部分溶液粘到瓶壁和瓶塞上,所以溶液的浓度不变,
故答案为:=.
点评 本题考查了物质的量浓度的有关计算、一定物质的量浓度溶液配制及误差分析等知识点,难度中等,明确配制原理及操作步骤是解题关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2O是淡黄色固体,和水反应生成NaOH,是碱性氧化物 | |
| B. | 钠应保存于煤油中 | |
| C. | 钠投入滴有紫色石蕊试液的水中,溶液呈现红色 | |
| D. | 钠的焰色为黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应是吸热反应 | |
| B. | 2mol甲醇所具有的能量是1451.6 kJ | |
| C. | 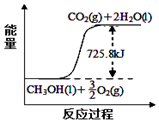 如图是CH3OH(l)燃烧反应过程的能量变化示意图 | |
| D. | 25℃、101kPa时,1 mol甲醇完全燃烧生成CO2和液态水,同时放出725.8 kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 需要加热才能发生的反应一定是吸热反应 | |
| C. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ/mol | |
| D. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,浓H2SO4与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
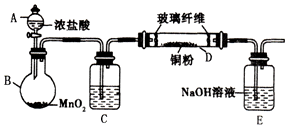 实验室采用如图所示的装置制取氯化铜(部分仪器和夹持装置已略去).
实验室采用如图所示的装置制取氯化铜(部分仪器和夹持装置已略去).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com