

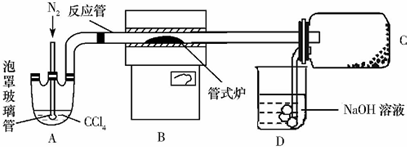
���� ��������ͼ֪���ظ���立ֽ������������������Cr2O3������ˮ����������ˮ��Ȼ��ϴ�ӡ���ɵõ�Cr2O3���ڼ��������£��ڷ�Ӧ���з�����ӦCr2O3+3CCl4�T2CrCl3+3COCl2�����Ȼ������������ڸ������ܱ�����������Ϊ��ֹ���Ȼ�����������ͨ�뵪�����ҳ���ĵ�����ʹ��Ӧ������ʽ¯�н��з�Ӧ�����õ���ˮ���Ȼ�����
��1���ظ���立ֽ������������������Cr2O3������ˮ����������ˮ�����ݵ����غ��ԭ���غ�д���˷ֽⷴӦ�Ļ�ѧ����ʽ���ظ���立ֽⲻ��ȫ�������ܺ����������������ʣ���Ϊ��NH4��2Cr2O7�Խۺ�ɫ�����Կ����ṩ��ɫ���жϣ�
��2����ΪCCl4�е�Ϊ76.8�棬�¶ȱȽϵͣ���˱�֤�ȶ���CCl4����������ͨ��ˮԡ������������������
��3�����������������Ȼ����ҳ��뵪����ʹ��Ӧ������ʽ¯�н��з�Ӧ��
��4�����ݹ�����ˮ�����CO2��HCl�ֱ���NaOH��Ӧ����Na2CO3��NaCl����д��NaOH��Һ���չ����Ļ�ѧ����ʽ��
��5��������Ȼ�������������ˮ�⣬�ڸ������ܱ��������������ʣ�����װ�ÿ�֪C��D֮��ȱ��һ������װ�ã�����ˮ������C�е������Ȼ���ˮ�⣮
��� �⣺��������ͼ֪���ظ���立ֽ������������������Cr2O3������ˮ����������ˮ��Ȼ��ϴ�ӡ���ɵõ�Cr2O3���ڼ��������£��ڷ�Ӧ���з�����ӦCr2O3+3CCl4�T2CrCl3+3COCl2�����Ȼ������������ڸ������ܱ�����������Ϊ��ֹ���Ȼ�����������ͨ�뵪�����ҳ���ĵ�����ʹ��Ӧ������ʽ¯�н��з�Ӧ�����õ���ˮ���Ȼ�����
��1���ظ���立ֽ������������������Cr2O3������ˮ����������ˮ��������Ӧ�Ļ�ѧ����ʽΪ����NH4��2Cr2O7$\frac{\underline{\;����\;}}{\;}$N2��+4H2O+Cr2O3����Ϊ��NH4��2Cr2O7�Խۺ�ɫ�����һ��ϴ�ӵ�����Һ����ɫ��˵��ϴ�Ӹɾ���
�ʴ�Ϊ����NH4��2Cr2O7$\frac{\underline{\;����\;}}{\;}$N2��+4H2O+Cr2O3�����һ��ϴ�ӵ�����Һ����ɫ��
��2����ΪCCl4�е�Ϊ76.8�棬�¶ȱȽϵͣ���˱�֤�ȶ���CCl4����������ͨ��ˮԡ�����������������������¶ȼ�ָʾ�¶ȣ�
�ʴ�Ϊ��ˮԡ���ȣ������¶ȼ�ָʾ�¶ȣ���
��3�����������������Ȼ����ҳ��뵪����ʹ��Ӧ������ʽ¯�н��з�Ӧ��Ϊ��ֹ���Ȼ�����������ʹ��Ӧ������ʽ¯�н��з�Ӧ�����뵪����
�ʴ�Ϊ���ٸϾ���Ӧװ���е�������
�ڹ���ʹ��Ӧ������ʽ¯�н��з�Ӧ��
��4�������ж���Ϊ��ֹȾ�ۻ�������NaOH��Һ���չ�������̼���ƺ��Ȼ��ƣ����ԭ���غ�ô˷�Ӧ�Ļ�ѧ����ʽΪCOCl2+4NaOH=Na2CO3+2NaCl+2H2O���ʴ�Ϊ��COCl2+4NaOH=Na2CO3+2NaCl+2H2O��
��5��Ϊ��ֹ���Ȼ���ˮ�⣬��װ��C��D֮������һ��ʢ�м�ʯ�ҵĸ���ܣ���U�ιܣ���
�ʴ�Ϊ����װ��C��D֮������һ��ʢ�м�ʯ�ҵĸ���ܣ���U�ιܣ���
���� ���⿼��ѧ���Ե�ʵ�鷽��ԭ�������������ۣ�Ϊ��Ƶ���㣬������ѧ���ķ���������ʵ�������Ŀ��飬��Ŀ�ѶȽϴ�����ʵ��ԭ���ǹؼ����Ƕ�ѧ���ۺ������뿼�飬��Ҫѧ���߱���ʵ�Ļ���֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��PX���Ļ�ѧʽΪC8H10���˴Ź�������ͼ����2�����շ� | |
| B�� | ��PX����ʹ���Ը��������Һ��ɫ�����ڱ���ͬϵ�� | |
| C�� | ��PX����һ�����Ͷ�������ͬ���칹��ֱ���1�֡�3�� | |
| D�� | ��PX��������ˮ���ܶȱ�ˮС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
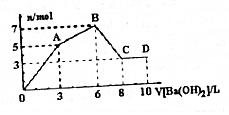 ��Al2��SO4��3��AlCl3�Ļ����Һ����μ���1mol/LBa��OH��2��Һ������������Ba��OH��2��Һ������������ó��������Ĺ�ϵ��ͼ������˵������ȷ���ǣ�������
��Al2��SO4��3��AlCl3�Ļ����Һ����μ���1mol/LBa��OH��2��Һ������������Ba��OH��2��Һ������������ó��������Ĺ�ϵ��ͼ������˵������ȷ���ǣ�������| A�� | ͼ��C����Ԫ�ش��ڵ���ʽ��AlO2- | |
| B�� | ԭ�����Һ��c[Al2��SO4��3]��c��AlCl3��=1��2 | |
| C�� | ��D����Һ��ͨ�����CO2���壬���ս��õ�9mol���� | |
| D�� | OA�η�Ӧ�����ӷ���ʽΪ��2Al3++3SO42-+3Ba2++6OH-�T2Al��OH��3��+3BaSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
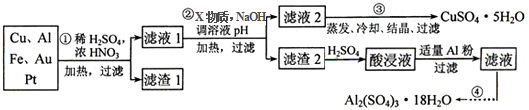
| �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.7 |
| Cu2+ | 4.9 | 6.7 |
| Al3+ | 3.0 | 4.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢� | C�� | �ۢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
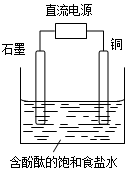
| A�� | ʯī�缫������Һ�ʺ�ɫ | B�� | ͭ�缫�Ϸ�����ԭ��Ӧ | ||
| C�� | ��Һ�е�Na+��ʯī�缫�ƶ� | D�� | ͭ�缫�����۲쵽����ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com