
����ͼ��ʾװ�ó�ȥ��CN����Cl����ˮ�е�CN��ʱ��������ҺpHΪ9~10��ij�缫�ϲ�����ClO����CN������Ϊ��������Ⱦ�����壬����˵����ȷ����
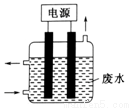
A��������ʯī����������������
B����ȥCN���ķ�Ӧ��2CN��+5ClO��+ 2H+ =N2��+2CO2��+5Cl��+H2O
C�������ĵ缫��ӦʽΪ��Cl��+2OH�� +2e��= ClO��+H2O
D�������ĵ缫��ӦʽΪ��2CN��+12OH�� ��10e��=N2��+2CO32��+6H2O

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�������и�����ѧ�����п������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ����д�����ý��۾���������
ѡ�� | ���ӷ���ʽ | ���� |
A | AgCl��s��+I-��aq���TAgI��s��+Cl-��aq�� | �ܽ�ȣ�AgI��AgCl |
B | Fe2++H2O2+2H+�TFe3++2H2O | �����ԣ�H2O2��Fe3+ |
C | CO32-+CO2+H2O�T2HCO3- | �ȶ��ԣ�HCO3-��CO32- |
D | NH3+H3O | ������������NH3��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���ຣʡ�߶���9���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ����ЧӦ��H����aq����OH����aq����HO��l������H����57��3kJ/mol����1L0��5mol?L-1 ��NaOH��Һ�м����������ʣ���ϡ�����ŨH2SO4����ϡ���ᣬǡ����ȫ��Ӧ����ЧӦ��H1����H2����H3�Ĺ�ϵ��ȷ����
A����H1����H2����H3
B����H1����H3����H2
C����H1����H3����H2
D����H1����H3����H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������һ�и�һ��ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ˮ������ˮʵ�����������ȷ����
A����ʵ��ı�װ�ð����IJ��������У��ƾ��ơ�Բ����ƿ��ֱ�������ܺ���ƿ
B����������ʵ�飬װ���ڲ�Ӧ�����������ͨ�Ա�֤��ȫ
C������ˮӦ�ô��¿ڽ����Ͽڳ�
D��ʵ�����ʱӦ����Ϩ��ƾ��ƣ���ֹͣͨ����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������������ڽ�����������
A���˵��в˺�ϴ���ͷŻص��� B���������Ƴɲ����
C���������ı��������� D�����ڵ��µĸֹ���п������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ���˲�һ�и�����10��������ѧ�Ծ��������棩 ���ͣ�ѡ����
������������ָ������Һ���ܴ����������
A�������۷�Ӧ�ų�H2����ɫ��Һ��NO3-��Al3����Na����SO42-
B��ʹ��ɫʯ����ֽ��������Һ��SO42-��HCO3-��Na����K��
C��������Һ��Fe3����Al3����NO3-��SO42-
D��������c��H+��/c��OH-����1��10-12����Һ��K����AlO2-��CO32-��Na��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������˫Ѽɽ��һ��ѧ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ������Cu��Fe2O3�Ļ�����м���100 mL 2 mol��L��1�����ᣬǡ��ʹ�������ȫ�ܽ⣬������Һ�в���Fe3�������ù�����CO�ڸ����»�ԭ��ͬ������ԭ����������ٵ�����Ϊ
A��3.2 g B��2.4 g C��1.6 g D��0.8 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����������£����и���ˮ�м���FeSO4���ɽ��к���Cr2O72-ת��Ϊ Cr3+��Ȼ���ټ�����ʯ�ҵ�����Һ��pH��ʹCr3+ת��ΪCr��OH��3���������ӷ�ˮ�г�ȥ������˵����ȷ����
A��FeSO4�ڷ�Ӧ����������
B�����ŷ�Ӧ�Ľ��У��÷�ˮ��pH���С
C�����÷�Ӧת��0.6mol e-�������0.2mol Cr2O72- ����ԭ
D����ȥ��ˮ�к���Ԫ�����ӵĹ��̰���������ԭ��Ӧ���ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ĵ�ʡ�Ű��и���9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ǻ�ѧѧϰ���о��ij����ֶΣ����з������ݺͽ��۶���ȷ����
A�������ᡢ���â������ʯ�ҷֱ������ᡢ��Ρ�������
B��HClO��H2SO4��Ũ����HNO3������ǿ�����ԣ�������������
C��Ư�ۡ��������֡���ˮ����ˮ����ˮ��Ϊ�����
D�� Na2O��NaOH�� NaCl��Na2SO4��Na2O2�������Ƶĺ���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com