
【题目】下列事实不能用元素周期律知识解释的是
A. 非金属性:O > S B. 稳定性:HCl >H Br
C. 酸性:HCl > H2CO3 D. 碱性: LiOH <NaOH
科目:高中化学 来源: 题型:
【题目】下列说法正确的是:( )
A.在100℃、101kpa条件下,液态水的气化热为40.69kJ/mol,则H2O(g) ![]() H2O(l)的△H=40.69kJ/mol
H2O(l)的△H=40.69kJ/mol
B.已知MgCO3的Ksp=6.82×10-6,则所有含有固体的溶液中,都有c(Mg2+)=c(CO32-)=6.82×10-6
C.已知: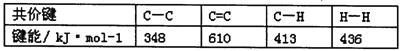 ,则可以计算出反应
,则可以计算出反应 的△H为-384kJ/mol
的△H为-384kJ/mol
D.常温下,在0.10mol/L的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数,下列说法正确的是
A.标准状况下,22.4 L水中含有的水分子数为NA
B.常温常压下,46 g NO2和N2O4的混合气体中含有的氧原子数为2NA
C.1mol/L的Ba(NO3)2溶液中含NO3-离子数为2NA
D.分子数为NA的CO和N2的混合气体的体积约为22.4 L,质量为28 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于DNA与RNA的叙述,正确的是( )
A. 在细胞内存在的主要部位相同 B. 构成的五碳糖不同
C. 核苷酸之间的连接方式不同 D. 构成的碱基相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示, 该气体所含原子总数为________个,该气体在标准状况下的体积为________L。
(2) 在标准状况下,由CO和CO2组成的混合气体为67.2 L,质量为120 g,此混合物中CO和CO2物质的量之比是________, CO的质量是________,混合气体的平均摩尔质量是 。
(3)若40 g密度为ρ g·cm-3的硝酸钙溶液里含2 g Ca2+,则NO![]() 的物质的量浓度是____________。
的物质的量浓度是____________。
(4)将标准状况下的VL氨气溶于100g水中,得到的氨水密度为ag/cm3,则该溶液的物质的量浓度为 。
(5)标准状况下,现有①6.72 L CH4 ②3.01×1023个HCl分子 ③13.6 g H2S ④0.2 mol NH3,对这四种气体的关系有以下四种表述:其中正确的是____________
a.体积:②>③>①>④ b.物质的量:②>③>④>①
c.质量:②>③>①>④ d.氢原子个数:①>③>④>②
(6)按体积比为1:2:3所组成的N2、O2、CO2,混合气体20g在标准状况下体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4 mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65 kJ的热量。
(1)写出肼和过氧化氢的结构式:肼____________过氧化氢____________。
(2)写出反应的热化学方程式:__________________________。
(3)已知H2O(l)===H2O(g) ΔH=+44 kJ·mol-1,则16 g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是________kJ。
(4)上述反应用于火箭推进剂,除释放大量热和快速产生大量气体个很突出的优点是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不正确的是( )
A.共价化合物中不可能含有离子键
B.H2O比H2S稳定,H—S键比H—O键更难断裂
C.最外层只有一个电子的原子与卤素原子形成的化学键可能是离子键,也可能是共价键
D.离子键和共价键的实质都是电性的相互作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O (g)。半水煤气经过下列步骤转化为合成氨的原料。完成下列填空:
![]()
(1)半水煤气含有少量硫化氢。将半水煤气样品通入 溶液中(填写试剂名称),出现 ,可以证明有硫化氢存在。
(2)写出半水煤气在铜催化下实现CO变换的反应方程式 ;若半水煤气中V(H2): V(CO): V(N2)=9:7:4,经CO变换后的气体中:V(H2): V(N2)=__________。
(3)碱液吸收法是脱除二氧化碳的方法之一。有一吸收了二氧化碳的氢氧化钠洛液,为测定其溶液组成,采用双指示剂法进行滴定。
步骤:用移液管量取V0mL的该溶液于锥形瓶中,先滴入1-2滴酚酞做指示剂,滴定达到终点时用去c mol.L-1的标准盐酸溶液VlmL,此时再向溶液中滴入1-2滴__________做指示剂,达到滴定终点时又用去V2mL标准盐酸溶液。
第二次滴定达到终点时的现象是______________________。
数据处理:通过Vl和V2的相对大小可以定性也可定量判断溶液的组成。
若V1>V2,写出此时的溶质的化学式_______________。
若2V1=V2,写出此时溶液中离子浓度由大到小的顺序_________________。
讨论:若V1<V2,在第一次滴定时未用标准盐酸润洗酸式滴定管,第二次滴定前发现并纠正了错误,则____________(填化学式)浓度偏大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列离子方程式的说法正确的是( )
A.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
B.向NaAlO2溶液中通入少量的CO2的反应为:2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32—
C.FeBr2与足量的Cl2反应为:2Fe2++2Br—+2Cl2=2Fe3++Br2+4Cl—
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO4—+6H++5H2O2=2Mn2++5O2↑+8H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com