
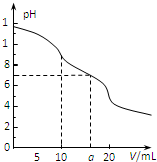
 常温下,用 0.1mol?L-1 HCl溶液滴定10.0mL浓度为0.1mol?L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法不正确的是( )
常温下,用 0.1mol?L-1 HCl溶液滴定10.0mL浓度为0.1mol?L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法不正确的是( )| A、当V=0时:c(H+)+c(HCO3-)+2c(H2CO3)=c(OH-) |
| B、当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-) |
| C、当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| D、当V=a时:c(Na+)>c(Cl-)>c(H+)=c(OH-) |


科目:高中化学 来源: 题型:
| A、① | B、② | C、③ | D、④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸馏使沸点低液体蒸出 |
| B、过滤除去不溶性杂质 |
| C、加热使杂质分解成气体 |
| D、萃取分液使溶质转移到另一溶剂中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
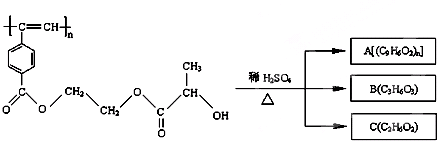
| A、M、A均能使酸性高锰酸钾溶液和溴水褪色 |
| B、B中含有羧基和羟基两种官能团,B能发生消去反应和酯化反应 |
| C、1molM与热的烧碱溶液反应,可消耗2n mol的NaOH |
| D、A、B、C各1mol分别与金属钠反应,放出的气体的物质的量之比为1:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、放电时负极:Cd-2e-=Cd2+ |
| B、充电时阳极:Cd(OH)2+2e-=Cd+2OH- |
| C、充电时阳极:2Ni(OH)2-2e-+4H+=2Ni3++4H2O |
| D、放电时正极:2NiOOH+2e-+2H2O=2Ni(OH)2+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应速率可表示可逆反应进行的程度 |
| B、根据化学反应速率的大小可知化学反应进行的快慢 |
| C、化学反应速率是指一定时间内,任何一种反应物浓度的减少或任何一种生成物浓度的增加 |
| D、对于任何化学反应来说,反应速率越大,反应现象越明显 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2 |
| B、N2O |
| C、NO |
| D、NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 | B、11 | C、12 | D、13 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com