4.某化学兴趣小组的同学欲利用如图所示装置验证浓硝酸与木炭反应时有NO
2、CO
2生成,并探究是否还有NO生成.(已知:NO
2的沸点为21.1℃,NO的沸点为-151℃,CO
2的沸点为-78.5℃;酸性KMnO
4溶液能将NO氧化成为NO
3-.)
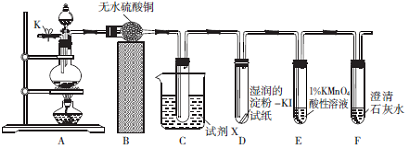
(1)装置经气密性检查后加入试剂并连接好仪器,然后打开开关K,通过导管向装置内通入氮气,其目的是排出装置内的空气,防止其对NO的检验的干扰.
(2)实验中用无水CuSO
4代替无水CaCl
2干燥气体的一个好处是可判断水蒸气是否全部被吸收;装置C用于检验、收集并除去NO
2,试剂X是冰水(填名称),装置D的作用是检验二氧化氮是否已全部除去.
(3)若装置E中溶液的颜色慢慢褪去,则E中发生反应的离子方程式是5NO+3MnO
4-+4H
+=5NO
3-+3Mn
2++2H
2O;若装置E中没有明显的变化,装置C和F出现了预期的现象,则装置A中发生反应的化学方程式为C+4HNO
3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO
2↑+4NO
2↑+2H
2O;若装置E、F中的试剂对调,则能(填“能”或“不能”)达到预期的实验目的,其判断理由是因为二氧化碳与酸性高锰酸钾溶液不反应,NO与石灰水不反应、
(4)将等物质的量的NO
2、NO混合后通入低温下的水中只得到一种含氧酸X,该酸的化学式可能为HNO
2.请设计一种实验方案,以确定含氧酸X与碳酸的酸性相对强弱:向装有碳酸氢钠的试管里滴加亚硝酸溶液,若有气泡产生,则亚硝酸的酸性相对较强,若无气泡产生,则亚硝酸的酸性相对较弱,或比较等物质的量浓度的亚硝酸钠溶液、碳酸氢钠溶液的PH大小,PH小的,对应的酸的酸性相对较强.