
用 NA 表示阿伏伽德罗常数的数值,下列叙述正确的是
A.常温下,1 mol丙烯中含碳原子数为3 NA
B.常温下,pH=13的NaOH溶液中含OH?数为NA
C.标准状况下,22.4L CHCl3 中含C-H键数为NA
D.23g Na与足量氧气反应时转移的电子数为2 NA
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:实验题
(10分) NaHCO3是重要的化工原料,在实验室里可通过下列两个步骤得到:
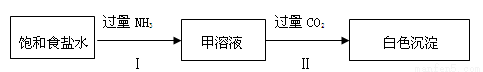
已知一些物质在20℃、30℃时溶解度数据:
温度(℃) | NH4Cl | NH4HCO3 | NaHCO3 | NaCl | Na2CO3 | (NH4)2CO3 |
20 | 28.7 | 21.7 | 9.6 | 31.5 | 21.5 | 100 |
30 | 41.1 | 27.0 | 11.1 | 36.3 | 39.7 | >100 |
请回答:
(1)步骤Ⅰ反应的化学方程式是 。
(2)若将NH3和CO2两种气体通入顺序互换后没有沉淀,原因是 。
(3)步骤Ⅱ所得白色沉淀中一定有NaHCO3,原因是 。
(4)步骤Ⅱ生成NaHCO3的离子方程式是 。
(5)根据气体物质溶解性及上列溶解度数据,简述上述两过程在较低温度下进行时效果更好的原因 。
查看答案和解析>>
科目:高中化学 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
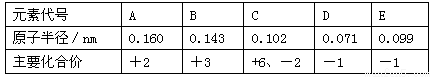
A.A、B的单质与稀盐酸反应速率B>A
B.D、E形成的简单离子的还原性E->D-
C.气态氢化物的稳定性HD<H2C
D.最高价氧化物对应的水化物的酸性 H2CO4>HEO4
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市高三上学期9月质量检测化学试卷(解析版) 题型:填空题
(9分)氮的氧化物对人体危害极大,实验时应防止其对空气的污染。
实验一:某同学利用下列装置实现铜与浓硝酸、稀硝酸的反应。
Ⅰ、取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ、将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ、按如图所示装置连接仪器、检查气密性、装入化学试剂。

(1)请完成过程Ⅰ发生反应的离子方程式:
Cu2(OH)2CO3+4H+= 。
(2)过程Ⅲ的后续操作如下:
① 为使浓硝酸与铜丝接触,操作是打开止水夹a和b, ,当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器。生成红棕色气体的化学方程式是 。
② 控制b与分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见有无色气体产生。稀硝酸充满玻璃管的目的是 。
实验二:NO2与水反应的实验研究。
(3)将3支充满红棕色气体的小试管分倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):
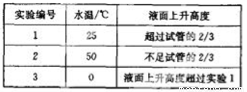
① 根据上表得出的结论是温度越 (填“高”或“低“),进入试管中的溶液越多。
② 查阅材料:a.NO2与水反应的实际过程为:2NO2+ H2O=HNO3+ HNO2,3 HNO2= HNO3+2NO↑+H2O;b. HNO2不稳定。则产生上述现象的原因是 。
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市高三上学期9月质量检测化学试卷(解析版) 题型:选择题
实验室某些物质的制备装置如图所示(省略夹持装置和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的是
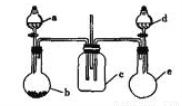
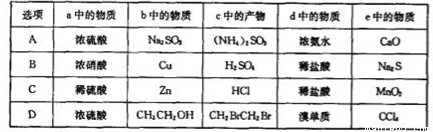
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市宁城县高三上学期摸底统一考试化学试卷(解析版) 题型:填空题
(15分)【化学-有机化学基础】A与B在一定条件下反应生成C,进一步反应生成抗氧化剂“安维那”D,其分子式为C10H10O4。A对氢气的相对密度为52,1 mol A与足量NaHCO3反应生成2 mol气体。B属于芳香类化合物。已知:
RCHO+CH2(COOH)2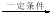 RCH=C(COOH)2+H2O,
RCH=C(COOH)2+H2O,
RCH=C(COOH)2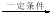 RCH=CHCOOH+CO2
RCH=CHCOOH+CO2
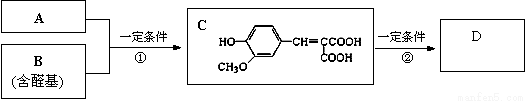
(1)C可能发生的反应是____________(填序号)。
A.氧化反应 B.水解反应 C.消去反应 D.酯化反应
(2)等物质的量的C分别与足量的Na、NaHCO3、NaOH反应时消耗Na、NaHCO3、NaOH的物质的量之比是_____________。
(3)A的分子式是____________。
(4)反应①的化学方程式是______________________________________________________。
(5)符合下列条件的D的同分异构体有_______种,写出其中任意一种的结构简式______________。
①在苯环上只有两个取代基;
②在苯环上的一氯取代物只有两种;
③1 mol该同分异构体与足量NaHCO3反应生成2 mol CO2。
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市宁城县高三上学期摸底统一考试化学试卷(解析版) 题型:选择题
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如下图所示。
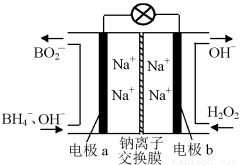
下列说法错误的是( )
A.电池放电时Na+从a极区移向b极区
B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.该电池的负极反应为:BH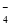 +8OH--8e-=BO
+8OH--8e-=BO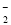 +6H2O
+6H2O
D.每消耗3 mol H2O2,转移的电子为3 mol
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古巴彦淖尔市高三10月月考化学试卷(解析版) 题型:选择题
已知下列热化学方程式:
Zn(s)+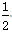 O2(g)===ZnO(s) ΔH1=-351.1 kJ/mol
O2(g)===ZnO(s) ΔH1=-351.1 kJ/mol
Hg(l)+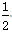 O2(g)===HgO(s) ΔH2=-90.7 kJ/mol
O2(g)===HgO(s) ΔH2=-90.7 kJ/mol
由此可知Zn(s)+HgO(s)===ZnO(s)+Hg( l) ΔH3,其中ΔH3是
A.-441.8 kJ/mol B.-254.6 kJ/mol
C.-260.4 kJ/mol D.-438.9 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古高二下学期期末考试化学试卷(解析版) 题型:选择题
升高温度,下列数据不一定增大的是
A.化学反应速率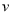 B.KNO3的溶解度S
B.KNO3的溶解度S
C.化学平衡常数K D.水的离子积常数KW
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com