
| ��ѧ�� | C-H | C�TC | C-C | H-H |
| ����/kJ•mol-1 | 414.4 | 615.3 | 347.3 | 435.3 |
���� ��1�������Ȼ�ѧ����ʽ����д������֪����ѧ�������뷴Ӧ�ȳ����ȣ���ע��������ʵľۼ�״̬�����
��2�����ݷ�Ӧ�ȵ��ڷ�Ӧ����ܼ���-��������ܼ������㣻
��3�������ȸ��ݷ�Ӧ�����������д��ѧ����ʽ�����ݸ�˹���ɼ��㷴Ӧ���ʱ䣬�������Ȼ�ѧ����ʽ����д��������д�Ȼ�ѧ����ʽ��
��� �⣺��1��5gCH3OH��������ȼ������CO2��Һ̬ˮ���ų�113.5kJ������64g��1molCH3OH��������ȼ������CO2��Һ̬ˮ���ų�1452.8kJ������
���Ȼ�ѧ����ʽΪ��2CH3OH��g��+3O2��g���T2CO2��g��+4H2O��l����H=-1452.8KJ/��
�ʴ�Ϊ��2CH3OH��g��+3O2��g���T2CO2��g��+4H2O��l����H=-1452.8KJ/mol��
��2���ڷ�ӦCH3-CH3��CH2=CH2+H2�У�����6mol C-H����1mol C-C�������յ�����Ϊ��6��414.4kJ+347.4kJ=2833.8kJ��
����1molCH2=CH2��1molH2�����γ�4molC-H����1molC=C��1molH-H�����ų�������Ϊ��4��414.4kJ+615.3kJ+435.3kJ=2708.2kJ��
���յ������࣬�ų��������٣��÷�ӦΪ���ȷ�Ӧ�����յ�����Ϊ��2833.8kJ-2708.2kJ=125.6�����Է�Ӧ��Ϊ+125.6kJ/mol��
�ʴ�Ϊ��+125.6kJ/mol��
��3����֪����C ��s��ʯī��+O2��g��=CO2��g����H1=-393kJ•mol-1��
��2H2��g��+O2��g��=2H2O ��l����H2=-571.6kJ•mol-1��
��2C2H2��g��+5O2��g���T4CO2��g��+2H2O ��l����H2=-2599kJ•mol-1��
2C ��s��ʯī��+H2��g��=C2H2��g���ķ�Ӧ���Ը��ݢ١�2+�ڡ�$\frac{1}{2}$-�ۡ�$\frac{1}{2}$�õ���
���Է�Ӧ�ʱ��H=2����-393kJ•mol-1��+��-571.6kJ•mol-1����$\frac{1}{2}$-��-2599kJ•mol-1����$\frac{1}{2}$=+227.7kJ•mol-1��
�ʴ�Ϊ��+227.7kJ•mol-1��
���� ���⿼��ѧ����˹���ɵ�Ӧ�ú��Ȼ�ѧ����ʽ����д�����֪ʶ��ע�ⷴӦ�ȵ��ڷ�Ӧ����ܼ���-��������ܼ��ܡ���˹���ɵ�Ӧ�ã�


 ����ͬ�����Ծ�ϵ�д�
����ͬ�����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
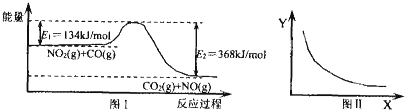
| A�� | �÷�Ӧ���ʱ��H=+234 kJ•mol-1 | |
| B�� | ��X��ʾ�¶ȣ���Y��ʾ�Ŀ�����CO2�����ʵ���Ũ�� | |
| C�� | ��X��ʾCO����ʼŨ�ȣ���Y��ʾ�Ŀ�����NO2��ת���� | |
| D�� | ��X��ʾ��Ӧʱ�䣬��Y��ʾ�Ŀ����ǻ��������ܶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
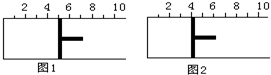 ��ͼ��ʾ��һ�������½�lmolA�����3molB�������һ������ɱ���ܱ������У��ɻ���������λ��ͼ1��ʾ���ں��º�ѹ�·���A��g��+3B��g��?2C��g��������Ӧ�ﵽƽ��ʱ������λ����ͼ2��ʾ����ƽ��ʱA��ת����Ϊ��������
��ͼ��ʾ��һ�������½�lmolA�����3molB�������һ������ɱ���ܱ������У��ɻ���������λ��ͼ1��ʾ���ں��º�ѹ�·���A��g��+3B��g��?2C��g��������Ӧ�ﵽƽ��ʱ������λ����ͼ2��ʾ����ƽ��ʱA��ת����Ϊ��������| A�� | 20% | B�� | 40% | C�� | 50% | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ | B�� | ѹǿ | C�� | �ܶ� | D�� | ƽ��Ħ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
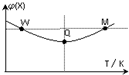 ��2L�����ܱ������г���2mol X��1mol Y������Ӧ��2X��g��+Y��g��?3Z��g����H��0����Ӧ���̳��������¶ȣ���û����ϵ��X������������¶ȵĹ�ϵ��ͼ��ʾ�������ƶ���ȷ���ǣ�������
��2L�����ܱ������г���2mol X��1mol Y������Ӧ��2X��g��+Y��g��?3Z��g����H��0����Ӧ���̳��������¶ȣ���û����ϵ��X������������¶ȵĹ�ϵ��ͼ��ʾ�������ƶ���ȷ���ǣ�������| A�� | �����¶ȣ�ƽ�ⳣ������ | |
| B�� | W��X������Ӧ����С��M��X������Ӧ���� | |
| C�� | Q��ʱ��Y��ת������С | |
| D�� | ƽ��ʱ����Z���ﵽ��ƽ��ʱZ�����������ԭƽ��ʱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ���� | ��������������mL�� | NaOH��Һ��Ũ�ȣ�mol•L-1�� | �ζ����ʱ��NaOH��Һ����������mL�� |
| 1 | 20.00 | 0.10 | 24.18 |
| 2 | 20.00 | 0.10 | 23.06 |
| 3 | 20.00 | 0.10 | 22.96 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
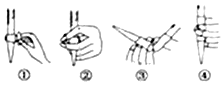
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Һ���У�pN=7 | |
| B�� | ������Һ���У�c��NH4+��•c��NH2-����1.0��10-14 | |
| C�� | 1 L�ܽ���0.001 mol NH4C1��Һ����Һ����pN=3 | |
| D�� | 1 L�ܽ���0.001 mol NaNH2��Һ����Һ����pN=11 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com