
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢或锂电池的十倍,可连续使用一个月才充一次电,其电池反应为: ,则下列有关说法不正确的是
,则下列有关说法不正确的是
A、放电时化学能转变为电能 B、放电时 参与正极反应
参与正极反应
C、充电时阴极产生 D、充电时每生成1mol
D、充电时每生成1mol ,则转移6mol电子
,则转移6mol电子
科目:高中化学 来源: 题型:
某课外学习小组的同学设计了如图的装置,以验证SO2的氧化性、还原性和漂白性。

请回答以下问题:
(1)用Na2SO3固体粉末和稀硫酸溶液制取SO2气体,应选用_____(选“A”或“C”)。
(2)课外学习小组的同学用FeS固体(块状,不溶于水)和稀硫酸制取H2S气体,反应的方程式为FeS + H2SO4 = FeSO4 + H2S↑,应选用_____(选“A”或“C”)做气体发生装置。请说出上述两个反应选取装置的理由 。
(3)SO2气体通过D装置时现象是 ,通过E装置时现象是 ;SO2与H2S在B装置中反应,现象是__________。
(4)F中盛有碱石灰,其作用是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合气体中可能含有Cl2 、O2 、SO2 、NO 、NO2 中的两种或多种气体。现将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是 ( )
A.肯定有SO2 和NO B.肯定有Cl2 、O2和NO2
C.可能有Cl2和O2 D.肯定只有NO
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、 等杂质。某同学设计了 如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3,的质量分数(忽略NH3在强碱性溶液中的溶解)。
等杂质。某同学设计了 如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3,的质量分数(忽略NH3在强碱性溶液中的溶解)。
(1)实验原理
①Al4C3与硫酸反应可生成CH4;
②AlN溶于强酸产生铵盐,溶于强碱生成氨气,请写出AlN与NaOH溶液反应的化学方程式 。
(2)实验装置(如图所示)

(3)实验过程
①连接实验装置,检验装置的气密性。称得D装置的质量为
 ,滴定管的读数为
,滴定管的读数为 mL。
mL。
②称取x g AlN样品置于锥形瓶中;塞好胶塞,关闭活塞K2、K3,打开活塞 ,通过分液漏斗加入稀硫酸,与烧瓶内物质充分反应。
③待反应进行完全后,关闭活塞K1,打开活塞K3,通过分液漏斗加入过量 (填化学式),与烧瓶内物质充分反应。
④ (填入该步应进行的操作)。
⑤记录滴定管的读数为 mL,称得D装置的质量为
mL,称得D装置的质量为
 ,
,
(4)数据分析
①AlN的质量分数为 。
②若读取滴定管中气体的体积时,液面左高右低,则所测气体的体积 __________(填“偏大”、“偏小”或“无影响”)。
③ 的质量分数为 ___________。(该实验条件下的气体摩尔体积为
的质量分数为 ___________。(该实验条件下的气体摩尔体积为 )。
)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:①101 时,
时,
②稀溶液中: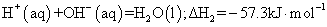
下列说中正确的是
A、若碳的燃烧热用 表示,则B、若碳的燃烧热用
表示,则B、若碳的燃烧热用 表示,则
表示,则
C、浓硫酸与稀 溶液反应的中和热值为57.3kJ·mol-1
溶液反应的中和热值为57.3kJ·mol-1
D、稀醋酸与稀 溶液反应生成1mol水,放出57.3kJ的热量
溶液反应生成1mol水,放出57.3kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碘与氢气反应的热化学方程式
(1) I2(g)+ H2(g)  2HI(g) △H = -9.48 kJ/mol
2HI(g) △H = -9.48 kJ/mol
(2) I2(S)+ H2(g)  2HI(g) △H = +26.48 kJ/mol
2HI(g) △H = +26.48 kJ/mol
下列判断正确的是 ( )
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(1)的产物比反应(2)的产物稳定
D.反应(2)的反应物总能量比反应(1)的反应物总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
沼气是一种能源,它的主要成分是CH4。0.5molCH4完全燃烧生成CO2和液态水时放出445kJ的热量,则下列热化学方程式中正确的是
A.2CH4(g) + 4O2(g) == 2CO2(g) + 4H2O(l) ΔH=+890kJ·mol-1
B.CH4(g) + 2O2(g) == CO2(g) + 2H2O(l) ΔH=+890kJ·mol-1
C.CH4(g) + 2O2(g) == CO2(g) + 2H2O(l) ΔH=-890kJ·mol-1
D.1/2CH4(g) + O2(g) == 1/2CO2(g) + H2O(l) ΔH=-890kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
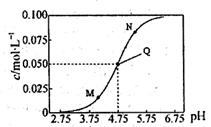
25℃时,满足c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的醋酸和醋酸钠混合溶液中,c(CH3COO-)与pH的关系如图所示。下列叙述错误的是
A.该温度下醋酸的电离常数Ka为l0-4.75mol·L-l
B.M点所表示的溶液中:
c(Na+)+c(H+)+c(CH3COOH)=0.1 mol·L-1
C.N点所表示的溶液中:
c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
D.Q点所表示的溶液中加入等体积的0.05mol·L-1NaOH溶液充分反应后pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
常温常压下,可能含有N2、 、CO、CO2的混合气体,依次通过足量的碳酸氢钠溶液和灼热的氧化铜,恢复到原来的温度和压强,气体体积没有变化;再通过足量的氧化钠,气 体积减少,最后通过灼热的铜网,恢复到原来的温度压强,体积又减少,并有剩余气体,若上述各步反应均完全,则对混合成分的判断正确的是( )
、CO、CO2的混合气体,依次通过足量的碳酸氢钠溶液和灼热的氧化铜,恢复到原来的温度和压强,气体体积没有变化;再通过足量的氧化钠,气 体积减少,最后通过灼热的铜网,恢复到原来的温度压强,体积又减少,并有剩余气体,若上述各步反应均完全,则对混合成分的判断正确的是( )
A、一定有N2和CO2,可能有 和CO
和CO
B、一定有N2,且 、CO、CO2中至少含有一种
、CO、CO2中至少含有一种
C、一定有N2、 、CO、CO2
、CO、CO2
D、一定有N2、CO、CO2,一定没有
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com