
【题目】[有机化学基础]
与有机物B相关的反应信息如下:
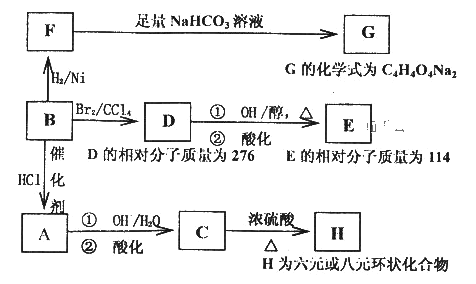
(1)写出下列反应的反应类型:
B→A______________,D→E第①步反应________________。
(2)写出E、C的结构简式:E_______________。C_______________。
(3)C的一种同分异构体K有如下特点:1molK可以和3mol金属钠发生反应放出33.6LH2(标准状况下),1molK可以和足量的NaHCO3溶液反应,生成1molCO2,1molK还可以发生银镜反应生成2molAg,试写出K的结构简式________________________。
(4)写出在浓硫酸存在并加热的条件下,F与足量乙醇反应的化学方程式_______________。
【答案】加成反应 消去反应 HOOCC![]() CCOOH
CCOOH 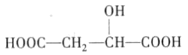
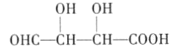
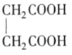 +2C2H5OH
+2C2H5OH![]()
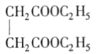 +2H2O
+2H2O
【解析】
由G的分子式可知,A~G各物质分子中均含有4个碳原子,由转化关系可以看出,B中含有不饱和键,B→A、B→F、B→D的反应均属于加成反应;A、D中均含有卤素原子,F中有羧基,根据G的分子式确定F为![]() ;根据反应条件可知D→E的第①步反应是卤代烃的消去反应;根据D、E的相对分子质量推知B、D、E分别为、HOOCCH=CHCOOH、HOOCCHBrCHBrCOOH、HOOCC
;根据反应条件可知D→E的第①步反应是卤代烃的消去反应;根据D、E的相对分子质量推知B、D、E分别为、HOOCCH=CHCOOH、HOOCCHBrCHBrCOOH、HOOCC![]() CCOOH,则A为HOOCCH2CHClCOOH,由此可知C为HOOCCH2CH(OH)COOH。由题给条件可看出,K中含有1个羧基,1个醛基,2个羟基。
CCOOH,则A为HOOCCH2CHClCOOH,由此可知C为HOOCCH2CH(OH)COOH。由题给条件可看出,K中含有1个羧基,1个醛基,2个羟基。
由G的分子式可知,A~G各物质分子中均含有4个碳原子,由转化关系可以看出,B中含有不饱和键,B→A、B→F、B→D的反应均属于加成反应;A、D中均含有卤素原子,F中有羧基,根据G的分子式确定F为![]() ;根据反应条件可知D→E的第①步反应是卤代烃的消去反应;根据D、E的相对分子质量推知B、D、E分别为、HOOCCH=CHCOOH、HOOCCHBrCHBrCOOH、HOOCC
;根据反应条件可知D→E的第①步反应是卤代烃的消去反应;根据D、E的相对分子质量推知B、D、E分别为、HOOCCH=CHCOOH、HOOCCHBrCHBrCOOH、HOOCC![]() CCOOH,则A为HOOCCH2CHClCOOH,由反应条件可知C为HOOCCH2CH(OH)COOH,
CCOOH,则A为HOOCCH2CHClCOOH,由反应条件可知C为HOOCCH2CH(OH)COOH,
(1)根据以上分析知B→A的反应类型为加成反应,D→E第①步反应的反应类型为消去反应;
故答案为:加成反应;消去反应;
(2)根据以上分析可知,E为HOOCC![]() CCOOH;C为
CCOOH;C为![]() ;
;
故答案为:HOOCC![]() CCOOH;
CCOOH;![]() ;
;
(3)C为HOOCCH2CH(OH)COOH,C的一种同分异构体K有如下特点:1mol K可以和足量的NaHCO3溶液反应,生成1molCO2,则含有1个羧基,1mol K可以和3mol金属钠发生反应放出33.6LH2(标准状况下),即1.5mol氢气,则还含有2个羟基,1molK还可以发生银镜反应生成2molAg,则含有1个醛基,又两个羟基不能连到同一个碳原子上,则K的结构简式为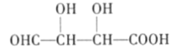
故答案为: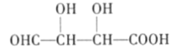 ;
;
(4)F为 ,与足量乙醇在浓硫酸存在并加热的条件下发生酯化反应,因为乙醇过量,两个羧基均发生反应,反应的化学方程式为
,与足量乙醇在浓硫酸存在并加热的条件下发生酯化反应,因为乙醇过量,两个羧基均发生反应,反应的化学方程式为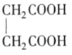 +2C2H5OH
+2C2H5OH![]()
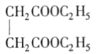 +2H2O;
+2H2O;
故答案为: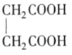 +2C2H5OH
+2C2H5OH![]()
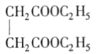 +2H2O。
+2H2O。


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
【题目】某课外活动小组收集了一种合金进行以下探究(已知铜元素的焰色反应呈绿色)。
(1)外观暗灰色,表皮光滑;
(2)在酒精灯外焰上灼烧,火焰呈绿色,合金片熔化,但不滴落;
(3)取刮去表皮的合金10 g,放入足量的稀硫酸中,收集到标准状况下的H2 8.96 L;
(4)另取刮去表皮的合金10 g,放入足量的NaOH溶液中,也收集到标准状况下的H2 8.96 L。
试据此判断,该合金中一定含有的元素是________(写元素符号);可能含有的元素是________(填选项编号)。
a.Ag b.Mg
c.Na d.Fe
如果该合金中只含2种元素,则二者的质量比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是合成某新型药物的中间体,下图是合成 G的部分流程:
已知:

乙酸酐的结构简式为![]()
请回答下列问题:
(1)G 中含氧官能团的名称是_______、________。
(2)反应 A→B 的化学方程式为________________。
(3)有机物 F的结构简式为_________________。
(4)反应 ④、⑤的反应类型分别是_________、___________。
(5)写出满足下列条件的 C 的同分异构体的结构简式______________________。
Ⅰ.苯环上只有两种取代基
Ⅱ.分子中只有 4 种不同化学环境的氢原子
Ⅲ.能与NaHCO3溶液反应生成 CO2
(6)以乙酸酐和![]() 为原料,制备
为原料,制备![]() 的部分流程图如下。请结合相关信息和已学知识,将合成路线补充完整(无机试剂任选)。
的部分流程图如下。请结合相关信息和已学知识,将合成路线补充完整(无机试剂任选)。
![]() ______________
______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图(反应条件和部分产物略去)。试回答:

(1)E的电子式是__________。
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是_________。
(3)物质Z常用于对空气进行杀菌、净化和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是__________________________。
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶液中各种离子的浓度由大到小的顺序是(不考虑H+)_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如下图:

请回答下列问题:
(1)配制溶液时,一般可以分为以下几个主要步骤:
①量取 ②计算 ③溶解 ④定容 ⑤转移 ⑥洗涤 ⑦装瓶,其正确的操作顺序为___________(填序号)。
(2)实验室只有100mL、250mL、500mL三种规格的容量瓶,但要配制480 mL 0.50 mol/L的稀硫酸,需取该浓硫酸______mL。
(3)接下来完成此实验你将用到的仪器有20mL量筒、烧杯、玻璃棒、____________。
(4)要从所配溶液中取出50 mL盛装于试剂瓶中,给它贴上标签,则标签的内容是________________;若再从中取出10 mL溶液稀释至20 mL,则稀释后溶液的物质的量浓度为__________。
(5)下列操作会使所配溶液浓度偏低的是__________。
A. 用量筒量取浓硫酸,读数时仰视刻度线 B. 转移溶液时未洗涤烧杯
C. 容量瓶用蒸馏水洗净后仍残留有蒸馏水 D. 定容时俯视容量瓶的刻度线
E. 定容摇匀后,发现液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是

A. 向苦卤中通入Cl2是为了提取溴
B. 粗盐可采用除杂和重结晶等过程提纯
C. 工业生产中常选用NaOH作为沉淀剂
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素铬(Cr)在自然界主要以+3价和+6价存在。
(1)+6价的Cr能引起细胞的突变而对人体不利,可用亚硫酸钠将其还原。离子反应方程式为:3SO32-+Cr2O72-+8H+===2Cr3++3SO42-+4H2O,该反应氧化剂和还原剂的物质的量之比为___________。
(2)工业上利用铬铁矿( FeO. Cr2O3)冶炼铬的工艺流程如图所示:
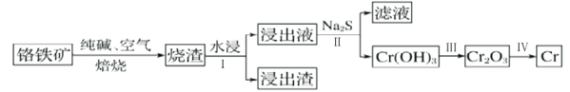
①为加快焙烧速率和提高原料的利用率,可采取的措施之一是___________。
②水浸Ⅰ要获得浸出液的操作是___________。
③浸出液的主要成分为Na2CrO4,加入Na2S反应后有Na2SO4生成,则操作Ⅱ发生反应的离子方程式为___________。
(3)常温下Cr(OH)3的溶度积Ksp=1×10-32,若要使Cr3+完全沉淀pH为___________[c(Cr3+)降至10-5mol·L-1可认为完全沉淀]。
(4)以铬酸钠(Na2CrO4)为原料,用电化学法可制备重铬酸钠(Na2Cr2O7),实验装置如图所示(已知:2CrO42-+2H+=Cr2O72-+H2O)。
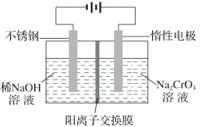
①阳极的电极反应式为___________。
②电解一段时间后,测得阳极区溶液中Na+物质的量由amol变为bmol,则生成重铬酸钠的物质的量为___________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,如图中的曲线可近似表示整个过程中混合溶液的导电能力变化的是(用电流强度I表示)

A. 曲线AB. 曲线BC. 曲线CD. 曲线D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为Fe2O3和CuO的混合物且氧化性强弱顺序:Fe3+>Cu2+>H+>Fe2+。X样品可发生如图所示的转化关系:
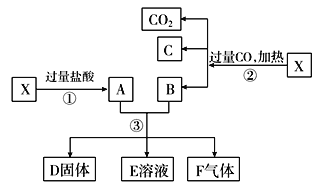
(1)写出步骤③可能发生反应的离子方程式:________________________(共有3个,任写一个即可)。
(2)若溶液E中只有一种金属离子,则一定是__________;若溶液E中含有两种金属离子,则一定是________。
(3)若D固体是纯净物,该固体是________(填化学式)。
(4)印刷电路板是由高分子材料和铜箔复合而成的,可用FeCl3溶液作“腐蚀剂”刻制印刷电路板,该过程发生反应的离子方程式为____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com