
| A����״���£�22.4 LCO2��O2��������к���6.02��1023����ԭ�� |
| B�����³�ѹ�£�0.1 mol����0.1 mol Cl2�г��ȼ�գ���1.806��1023������ת�� |
| C��һ�������£�2molSO2��1molO2��Ӧ��ƽ����ܱ������ڷ�����������1.204��1024 |
| D��1 L 1 mol/L��K2CO3��Һ�к���1.806��1024������ |
 ���ݼ���ϵ�д�
���ݼ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
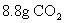 ��������
��������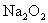 ������ȫ��Ӧ����������ȫ���ռ�����ֻ��1.68L����״��������������ڱ�״���µ��ܶ�Ϊ�� ��
������ȫ��Ӧ����������ȫ���ռ�����ֻ��1.68L����״��������������ڱ�״���µ��ܶ�Ϊ�� ��A��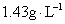 | B��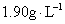 |
C��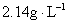 | D��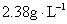 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A�� mol? mol? |
B�� ��10��3 mol? ��10��3 mol? |
C��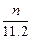 mol? mol? |
| D��cV mol? |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������£�4.4g CO2��N2O������������е�ԭ����ԼΪ0.3��6.02��1023 |
| B��������п��һ������Ũ�����ַ�Ӧ���ų�2.24L����ʱ��ת�Ƶ�����ԼΪ0.2��6.02��1023 |
| C����״���£�2.24L�����к��еķǼ��Լ���ԼΪ0.7��6.02��1023 |
| D����1mol��ԭ�ӵ�SiO2������Si��O���ĸ���ԼΪ2��6.02��1023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���Ȼ����Ħ����������NA���ȷ��Ӻ�NA������ӵ�����֮�� |
B�����³�ѹ��1 mol NO2������ˮ��Ӧ����NA��NO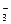 ���� ���� |
| C��121 g CCl2F2��������ԭ�Ӹ���Ϊ2NA |
D��62 g Na2O����ˮ��������Һ�к���O ������ΪNA ������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ��ϣ��ɰ�������ȫ��Ӧ�������Ʊ�V8O17����V2O3��V2O5�����ʵ���֮��ӦΪ�� ��
��ϣ��ɰ�������ȫ��Ӧ�������Ʊ�V8O17����V2O3��V2O5�����ʵ���֮��ӦΪ�� ��| A��1��2 | B��2��1 | C��3��5 | D��5��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1mol�����������NA��������ӵ�����֮����� |
| B��28g������40g���������ԭ����Ŀ��ȣ�����NA�� |
| C��2.3g����ԭ�ӱ�����ӣ�ʧȥ�ĵ�����Ϊ0.1NA |
| D��18g��ˮ��D2O�������ĵ�����Ϊ10NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��22.4L/mol��������Ħ����� |
| B���DZ�״���£�1mol�κ���������������Ϊ22.4L |
| C����״���£�22.4L�κ����嶼����Լ��6.02��1023������ |
| D��1molH2��O2�Ļ�������ڱ�״���µ������һ��Ϊ22.4L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ٺ͢ڶ���ȷ | B���ٺ͢۶���ȷ |
| C���ۺܶ͢���ȷ | D���ٺܶ͢���ȷ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com