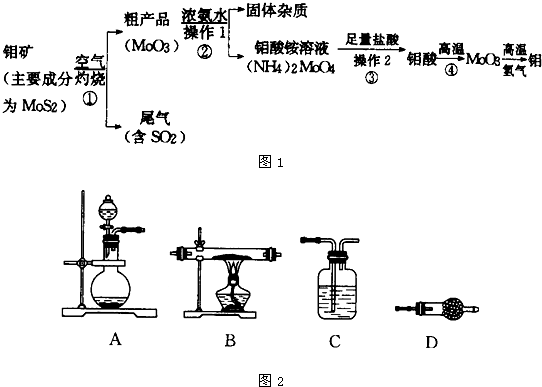
钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温强度及耐腐蚀性能.如图1所示是化工生产中制备金属钼的实验流程图:
(1)钼酸铵溶液中的阳离子检验方法:
.
(2)写出反应①的化学方程式.
.
(3)反应①的尾气可以NH
3?H
2O溶液吸收合成肥料,写出反应的离子方程式
.
(4)操作1中使用的主要玻璃仪器有
.
(5)某同学利用如图2所示装置来制备氢气,利用氢气还原三氧化钼,根据要求回答问题.
①请设计一个实验方案验证H
2的还原性并检验其氧化产物,其装置连接顺序是
.
②在烧瓶A中加入少量的硫酸铜目的是
.
②两次使用D装置,其中所盛的药品依次是
、
.



