
【题目】阿斯匹林(分子式为C9H8O4)是人们熟知的治感冒药,具有解热镇痛作用. 它的摩尔质量是( )
A.148g
B.148g/mol
C.180g/mol
D.146g
科目:高中化学 来源: 题型:
【题目】ClO2是一种优良的消毒剂,浓度过高时易发生分解,常将其制成NaClO2固体,以便运输和贮存,过氧化氢法制备NaClO2固体的实验装置如图1所示. 已知:2NaClO3+H2O2+H2SO4═2ClO2↑+O2↑+Na2SO4+2H2O
2ClO2+H2O2+2NaOH═2NaClO2+O2↑+2H2O
ClO2熔点﹣59℃、沸点11℃;H2O2沸点150℃
请回答:
(1)仪器A的作用是;冰水浴冷却的目的是(写两种).
(2)空气流速过快或过慢,均降低NaClO2产率,试解释其原因
(3)Clˉ存在时会催化ClO2的生成.反应开始时在三颈烧瓶中加入少量盐酸,ClO2的生成速率大大提高,并产生微量氯气.该过程可能经两步完成,请将其补充完整:①(用离子方程式表示),②H2O2+Cl2═2Cl﹣+O2+2H+ .
(4)H2O2浓度对反应速率有影响.通过图2所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备.该设备的作用是 , 馏出物是 .
(5)抽滤法分离NaClO2过程中,下列操作不正确的是
A.为防止滤纸被腐蚀,用玻璃纤维代替滤纸进行抽滤
B.先转移溶液至漏斗,待溶液快流尽时再转移沉淀
C.洗涤沉淀时,应使洗涤剂快速通过沉淀
D.抽滤完毕,断开水泵与吸滤瓶间的橡皮管,关闭水龙头.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有下列6种离子中的某几种:Cl﹣、SO42﹣、HCO3﹣、Na+、K+、Mg2+ , 所含离子的浓度均相等.为了确认溶液的组成,进行如下实验:取200mL上述溶液,加入足量Ba(OH)2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.88g,向沉淀中加入过量的盐酸,有2.33g.关于原溶液组成的结论,不正确的是( )
A.一定存在SO42﹣、HCO3﹣、Mg2+ , 至少存在Na+、K+中的一种
B.为了确定是否存在Cl﹣ , 可向溶液中加入硝酸酸化的硝酸银溶液
C.c(HCO3﹣)=0.05mol/L
D.4.88g沉淀中含有3种成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的NaCl溶液时,造成实验结果偏高的是( )
A.定容时观察液面仰视B.定容时观察液面俯视
C.盛溶液的烧杯未洗涤D.容量瓶中原来有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝粉与某些金属氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应.如:2Al+Fe2O3 ![]() 2Fe+Al2O3 , 反应发生时放出大量的热.仔细阅读上述信息回答下列问题:
2Fe+Al2O3 , 反应发生时放出大量的热.仔细阅读上述信息回答下列问题:
(1)“铝热反应”属于四种基本反应类型中的反应.
(2)信息中的“某些”指(填“比铝活泼的”“比铝不活泼的”或“任意”).
(3)试写出铝粉与MnO2发生的铝热反应方程式 .
(4)铝热反应可用于野外焊接钢轨,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油通过裂解可以得到乙烯,乙烯的产量可以用来衡量一个国家石油化工发展水平.如图是由乙烯为原料生产某些化工产品的转化关系图. 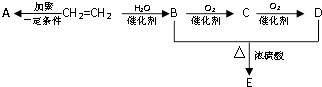
(1)乙烯生成B的反应类型是 .
(2)A的名称是 .
(3)C中含有的官能团是(填名称).
(4)写出B+D→E的化学反应方程式: .
(5)写出与E同类的任意两种同分异构体的结构简式、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是未来最理想的能源,科学家最近研制出利用太阳能产生激光,使海水分解得到氢气的新技术:
2H2O![]() 2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
(1)分解海水时,实现了从________能转变为________能。生成的氢气用于燃料电池时,实现________能转变为________能。水分解时,断裂的化学键为________键,分解海水的反应属于_______反应(填“放热”或“吸热”)。
(2)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:
A极:2H2+2O2--4e-===2H2O;B极:O2+4e-===2O2-
则A极是电池的________极;电子从该极________(填“流入”或“流出”)。
(3)有人以化学反应:2Zn+O2+4H+===2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是________,发生的电极反应为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如下表所示。下列判断正确的是( )

A. 原子半径:丙<丁<戊 B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊 D. 最外层电子数:甲>乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com