
| A.室温下,pH=3的氢氟酸加水稀释后,电离常数Ka(HF)和pH均减小 |
| B.室温下,将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) |
C.向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中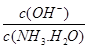 增大 增大 |
| D.室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊试液呈红色 |
科目:高中化学 来源:不详 题型:单选题
A.酸性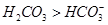 ,碱性 ,碱性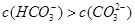 |
B.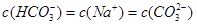 |
C.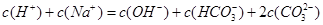 |
D.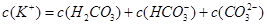 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 mol/L 硫酸溶液中H+浓度为2 mol/L |
| B.能跟锌反应产生氢气 |
| C.能使石蕊试液变红 |
| D.能与碳酸钠反应放出二氧化碳气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
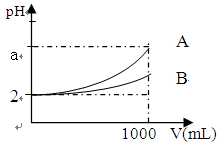
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 醋酸溶液加水稀释,下列说法正确的是()
醋酸溶液加水稀释,下列说法正确的是()| A.溶液中c(H+)和c(OH-)都减小 | B.溶液中c(H+)增大 |
| C.醋酸电离平衡向左移动 | D.溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
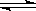 NH+OH-,下列情况能引起电离平衡向正向移动的有 ( )
NH+OH-,下列情况能引起电离平衡向正向移动的有 ( )| A.①③⑤ | B.①④⑥ | C.③④⑤ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
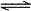 2H++SO32-
2H++SO32-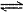 H3O++CO32-
H3O++CO32- 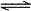 H2CO3+2OH-
H2CO3+2OH-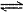 Ca2++CO32-
Ca2++CO32-查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com