
ˮϵ﮵�ؾ��а�ȫ�������ͼ۸�������ŵ��Ϊ��ǰ����о�������ȵ㡣�Է����ƣ�NaV3O8��Ϊ�������ϵĵ缫��ӦʽΪ��NaV3O8+xLi++xe��= NaLixV3O8��������˵������ȷ����

A���ŵ�ʱ�������ĵ缫��Ӧʽ��Li��e�� Li+
Li+
B����������Li��������������Ǩ��
C���������������ĵ缫��ӦʽΪNaLixV3O8��xe��=NaV3O8+xLi+��NaLixV3O8�з��Ļ��ϼ۷����仯
D���õ�ؿ�������������Һ�������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�����и�����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������������ȷ����
A����״���£�11.2 L SO3��������ԭ����Ϊ1.5NA
B����⾫��ͭʱ����������������6.4 g�����·��ת�Ƶ�����Ϊ0.2NA
C�����³�ѹ�£�4.0 g CH4�к��й��ۼ�����ĿΪNA
D���ں�Al3������ΪNA��AlCl3��Һ�У�Cl������Ϊ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015������ʡ�������и߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����±��������һ�������£��ܷ�����ȥ��Ӧ�Ҳ���ֻ��һ�ֵ���
A.CH3Cl B.CH3��CHBr��CH3
C.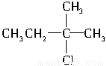 D.
D.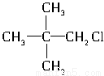
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��Ҵ�и�����������Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�ȡpH=2�����ֶ�Ԫ��H2A��H2B��1 mL���ֱ��ˮϡ�ͣ����pH�仯���ˮϡ�ͱ�������ͼ��ʾ�仯���������й���������ȷ����
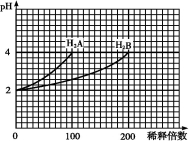
A��H2AΪ��Ԫǿ��
B��pH��4��NaHAˮ��Һ������Ũ�ȴ�СΪ��c(Na+)>c(HA-)>c(A2-)>c(H2A)>c(OH-)
C����NaHA��NaHB�Ļ����Һ�У�����Ũ�ȴ�СΪ��c(Na+)��c(A2-)��c(HB-)��c(B2-)��c(H2B)
D��Na2B��ˮ��Һ�У�����Ũ�ȴ�СΪ��c(Na+)>c(B2-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����и���ʮУ���������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
����16�֣���������CO2����Ч���Ƽ����Ч���õ��о�������ȫ��㷺��ע�����й�������������������ѧ�ҷ�����һ���µĿɽ�CO2ת��Ϊ�״��ĸ��Դ���ϵ����Ŀǰ��ҵʹ�õij����������90������CO2�Ʊ��״����̿����漰��Ӧ���£�
��Ӧ�� CO2(g)+3H2(g) CH3OH(g) +H2O(g) ��H 1=��49.58 kJmol-1
CH3OH(g) +H2O(g) ��H 1=��49.58 kJmol-1
��Ӧ��CO2(g)+ H2(g) CO (g)+H2O(g) ��H 2
CO (g)+H2O(g) ��H 2
��Ӧ�� CO(g)+2 H2(g) CH3OH(g) ��H 3=��90.77 kJmol-1
CH3OH(g) ��H 3=��90.77 kJmol-1
�ش��������⣺
��1����Ӧ��ġ�H 2= ����Ӧ���Է����������� ����ϵ��¡������ϸ��¡����κ��¶ȡ�����
��2����һ��������2L�����ܱ������г���һ������H2��CO2��������Ӧ��ʵ�����ڲ�ͬ��Ӧ����ʼͶ�����£���Ӧ��ϵ��CO2��ƽ��ת�������¶ȵĹ�ϵ���ߣ�����ͼ��ʾ��
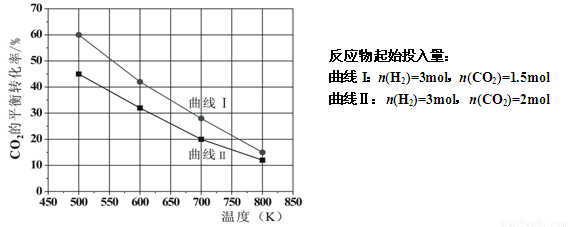
�پ�ͼ��֪����ҪʹCO2��ƽ��ת���ʴ���40%����������������ʵ��� ��
A��n(H2)=3mol��n(CO2)=1.5mol�� 650K
B��n(H2)=3mol��n(CO2)=1.7mol��550K
C��n(H2)=3mol��n(CO2)=1.9mol�� 650K
D��n(H2)=3mol��n(CO2)=2.5mol��550K
�����¶�Ϊ500K�������£�����3mol H2��1.5mol CO2���÷�Ӧ10minʱ�ﵽƽ�⣺
a����H2��ʾ�÷�Ӧ������Ϊ ��
b�����¶��£���ӦI��ƽ�ⳣ��K= ��
c���ڴ������£�ϵͳ��CH3OH��Ũ���淴Ӧʱ��ı仯������ͼ��ʾ������Ӧʱ��ﵽ3minʱ��Ѹ�ٽ���ϵ�¶�����600K������ͼ�л���3��10min��������CH3OHŨ�ȵı仯�������ߣ�

��3��ij�о�С�齫һ������H2��CO2��������ܱ������в�������ʵĴ�����������ӦI����
������˲�ͬ�¶�����ϵ�ﵽƽ��ʱCO2��ת���ʣ�a����CH3OH�IJ��ʣ�b������ͼ��ʾ����ش����⣺
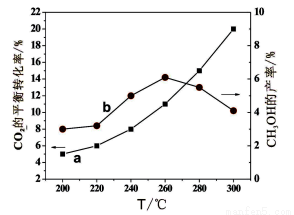
�ٸ÷�Ӧ�ﵽƽ���Ϊͬʱ��߷�Ӧ���ʺͼ״��������������´�ʩһ�����е��� ��ѡ���ţ���
A�����ø�Ч����
B�������¶�
C�����������
D��������״�
E������CO2��Ũ��
�ھ�ͼ��֪���¶ȸ���260���CO��Ũ�������¶ȵ����߶� �����������С���������䡱�����жϡ�������ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡЭ���������ѧ�����������ۺϻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
����ѧ��ѡ��5���л���ѧ��������15�֣���-����������-lapachone����һ�ֿ�����ҩ���ϳ�·�����£�
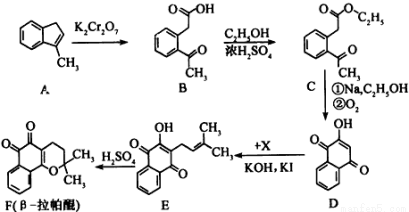
��1����֪X�ķ���ʽΪC5H9Cl����X�Ľṹ��ʽΪ��__________________
��2���л���B�Ĺ�����Ϊ��__________________�������ƣ�
��3��������Ӧ�У�ԭ�������ʴ�100%����( )��ѡ���A��B������B��C������D��E������E��F������
��4��D��E��������ȡ����Ӧ������һ�ָ�������E��Ϊͬ���칹�壬���������࣬�����ʵĽṹ��ʽΪ��______________________________��
��5��������B��ͬ���칹��ܶ࣬��������������ͬ���칹����Ŀ��_________�֣������������칹����
�ٱ�����������ȡ������
�ڷ�������һ��ȩ����һ���Ȼ���
�۷�����ֻ����һ������̼ԭ��
��6����֪��˫ϩ�ϳɷ�Ӧ��

��2-��-1��3-����ϩ����ϩΪԭ�ϣ����Լ����������ã��ϳɸ߷���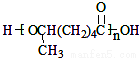 ��
��
��д������������Ӧ����ʽ��
2-��-1��3-����ϩ����ϩ��_____________________________________________________��
���ɸ߷���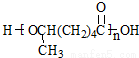 ��_________________________________��
��_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡЭ���������ѧ�����������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�����˵������ȷ����
A��������������ʵ���Ũ�ȵ�NaCl(aq) ������������NaClO(aq)����������
B��pH=3��������Һ��ˮ�ĵ���̶ȵ���pH=11�İ�ˮ��Һ��ˮ�ĵ���̶�
C��0��1 mol/L��NaHA��ҺpH��5������Һ��c(HA��)��c(H��)��c(A2��)��c(H2A)
D����NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ����û��Һ��c(Na��)��c(NH4��)��c(SO42��)��c(OH��)��c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ɽ��ʡԭƽ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����Ѫ�쵰���к���Fe2+���������ʳ�ÿ��������������Σ���ʹ���ж�����Ϊ�������λ�ʹFe2+ת��ΪFe3+�����ɸ���Ѫ�쵰��ɥʧ��O2�Ľ������������ά����C���Ի����������ε��ж�����˵��ά����C����
A������ B������ C�������� D����ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015������ʡ��������������У�߶���ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ������
��12�֣���1��ij�о���ѧϰС����ʵ����������1 mol/L��ϡ�������Һ��Ȼ������ζ�ijδ֪Ũ�ȵ�NaOH��Һ�������й�˵������ȷ����______________��
A��ʵ�������õ��ĵζ��ܡ�����ƿ����ʹ��ǰ����Ҫ��©��
B�����ʵ��������60 mL ϡ�������Һ������ʱӦѡ��100 mL����ƿ��
C������ƿ�к�����������ˮ���ᵼ���������Һ��Ũ��ƫС��
D����ʽ�ζ���������ˮϴ�Ӻ�װ���Ũ�ȵ�ϡ���ᣬ���õ�NaOH��Һ��Ũ�Ƚ�ƫ��
E���к͵ζ�ʱ���������һ�ζ���ʱ���Ӷ������������ʵ����ƫ��
��2�������£���֪0.1 mol��L��1һԪ��HA��Һ��c(OH��)/c(H+)��1��10��8��
�ٳ����£�0.1 mol��L��1 HA��Һ��pH= ��д�����ᣨHA����NaOH��Һ��Ӧ�����ӷ���ʽ�� ��
��pH��3��HA��pH��11��NaOH��Һ�������Ϻ���Һ��4���������ʵ���Ũ�ȴ�С��ϵ�ǣ� ��
��0.2 mol��L��1HA��Һ��0.1mol��L��1NaOH��Һ�������Ϻ�������Һ�У�c(H+)��c(HA)��c(OH��)�� mol��L��1������Һ����仯���Բ��ƣ�
��3��t��ʱ����pH=2��ϡ�����pH=11��NaOH��Һ�������Ϻ���Һ�����ԣ�����¶���ˮ�����ӻ�����Kw= �����¶��£�t�棩����100 mL 0.1 mol��L-1��ϡH2SO4��Һ��100 mL 0.4 mol��L-1��NaOH��Һ��Ϻ���Һ����仯���Բ��ƣ�����Һ��pH= ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com