
下列有关化学电源电极的叙述不正确的是( )。
A.锌锰碱性电池的负极材料为锌 B.铅蓄电池的负极材料为铅
C.镍镉电池的负极材料为镍 D.锂电池的负极材料为锂
科目:高中化学 来源: 题型:
微量元素硒(Se)对人体有保健作用,已知硒为第四周期第ⅥA族元素,根据它在周期表中的位置推测,下列对硒元素性质的描述不正确的是( )。
A.硒化氢不稳定 B.最高价氧化物的化学式是 SeO3
C.硒与铁反应可生成 FeSe D.酸性强弱顺序 HClO4>H3AsO4>H2SeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列组合判断正确的是 ( )
①Cl2具有很强的氧化性,在化学反应中只能作氧化剂 (2009·山东理综,10A)
②浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应 (2009·山东理综,13C改编)
③化合反应均为氧化还原反应 (2012·山东理综,7A)
④Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 (2012·山东理综,12A)
⑤Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应
(2012·山东理综,12C)
A.①②不正确
B.①②③④正确
C.①②正确,③④⑤不正确
D.①②③④⑤均不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,在下列溶液中发生如下反应:
①16H++10Z-+2XO ===2X2++5Z2+8H2O
===2X2++5Z2+8H2O
②2A2++B2===2A3++2B- ③2B-+Z2===B2+2Z-
由此判断下列说法正确的是 ( )
A.反应Z2+2A2+===2A3++2Z-不能进行
B.Z元素在①③反应中均被氧化
C.氧化性由弱到强的顺序是XO 、Z2、B2、A3+
、Z2、B2、A3+
D.还原性由强到弱的顺序是A2+、B-、Z-、X2+
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的值,下列说法中正确的是( )。
A、84gNaHCO3晶体中含有NA个CO32-
B、9.2gNO2和N2O4的混合气体中含有的氮原子数为0.2NA
C、标准状况下,11.2L臭氧中含NA个氧原子
D.标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)—空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%—30%的KOH溶液。电池总反应为:N2H4+O2=N2↑+2H2O。下列关于该燃料电池工作时的说法正确的是( )。
A.电池工作时,溶液中负极附近溶液的碱性增强,而电解质溶液pH减小
B.正极的电极反应式是:O2+4H++4e-=2H2O
C.负极的电极反应式是:N2H4+4OH――4e-=4H2O+N2↑ D.溶液中阴离子向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①将 通入酸性
通入酸性 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________.
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________.
A.  B.
B.  C.
C.  D.
D. 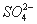
②亚硫酸钠中的硫呈+4价,它既有氧化性又有还原性,现在有试剂:溴水、H2S、稀硫酸。请选取合适的试剂证明Na2SO3具有还原性,并写出该反应的离子方程式为:_____________________________.
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由 、
、 、
、 、
、 组成。其中属于碱性氧化物的是______________________________。
组成。其中属于碱性氧化物的是______________________________。
②现取一份蛇纹石试样进行实验:
I. 先将其溶于过量的盐酸中、过滤,滤渣的主要成分是______________。
II. 再向滤液中加入 溶液至过量、过滤,滤渣中的主要成分是__________________。
溶液至过量、过滤,滤渣中的主要成分是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应A (g)+ 3B(g) = 2C(g) + 2D(g),下列数据表示反应进行得最快的是( )。
A.v(A)=0.7mol/(L·s) B.v (B) =1.8mol/(L · s)
C.v (C)=1mol/(L·s) D.v (D) =1.6mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
某原电池总反应离子方程式为2Fe3++Fe===3Fe2+,能实现该反应的原电池是( )
A.正极为Cu,负极为Fe,电解质溶液为Fe(NO3)2溶液
B.正极为Cu,负极为Fe,电解质溶液为FeCl3溶液
C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液
D.正极为Ag,负极为Fe,电解质溶液为CuSO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com