
将SO2和O2按物质的量之比2∶1充入具有适宜反应条件的容积固定的密闭容器内,SO2跟O2发生可逆反应.试分析说明在一定的时间里SO2、O2和SO3的物质的量浓度以及正反应速率和逆反应速率是怎样变化的.
|
分析:
①在反应即将开始的一瞬间,SO2和O2的浓度处于最大状态,它们合成SO3的速率也处于最大状态,SO3的浓度为0,它分解为SO2和O2的速率也是0,如图所示. ②反应开始后,SO2和O2的物质的量浓度逐渐减小,正反应速率逐渐减小,SO3的物质的量浓度逐渐增大,逆反应速率逐渐增大,如图所示. ③随着时间的延长,SO2和O2的物质的量浓度继续减小,正反应速率继续减小,SO3的物质的量浓度继续增大,逆反应速率继续增大. ④由于化学反应是可逆的,SO2和O2的物质的量浓度不会无限度的减小,而是变为某一个值后保持不变,正反应速率也不会无限度的减小而是变为某一个值后保持不变;SO3的物质的量浓度不会无限度的增大,而是变为某一个值后保持不变,逆反应速率也不会无限度的增大,而是变为某一个值后保持不变. ⑤在可逆反应里,既然是SO2、O2和SO3的物质的量浓度都保持不变,必然是在相同的时间内SO2、O2的生成浓度和减小浓度相等,SO3的生成浓度和减小浓度相等,即正反应速率和逆反应速率相等. |
|
在一定条件下,可逆反应2SO2+O2 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
为了除去工业废气中的SO2,某工厂采用下列措施:将经过初步处理的含有0.2%的SO2和10%的O2(均为体积分数)的废气,在400℃时,废气以5 m3/h的速度通过V2O5催化剂层后与20 L/h速度的NH3混合喷水。此时气体温度由800℃降至200℃,在热的结晶装置中得到(NH4)2SO4晶体(气体体积已折算成标准状态)。仔细阅读上文,回答问题:
(1)按反应理论值,SO2和O2的物质的量之比为2∶1,经过初步处理的废气中,SO2与O2的物质的量的比值为_________________,采用这样比值的原因是_________________。
(2)由计算说明为什么废气以5 m3/h速度与20 L/h速率的NH3混合?
查看答案和解析>>
科目:高中化学 来源: 题型:
为了除去工业废气中的SO2,将“SO2转化为(NH4)2SO4”的资料摘录如下:“一个典型的实例:初步处理后的废气中含0.2%的SO2和10%O2(体积比,下同)。400℃时将废气以5m3/h的速率通过V2O5催化剂层与20L/h的速率的氨气混合,再喷入水(290g/h),此时气体温度由400℃降为200℃。在热的结晶装置中可得到(NH4)2SO4晶体(气体体积均折算成标准状况)。”利用上述资料,用氨来除去工业废气中的SO2,回答下列问题:
(1)按反应中的理论值,SO2和O2的物质的量之比是2:1,该资料中的比值是
,简述不采用2:1的理由是 。
(2)通过计算,说明为什么废气以5m3/h的速率与20L/h的速率的氨气混合?
(3)若某厂每天排放1104m3这种废气,按上述方法该厂每月(按30天计算)可得硫酸铵多少吨?消耗氨气多少吨?
查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题

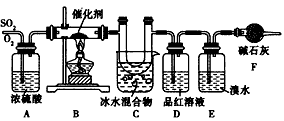
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com