
 石膏(CaSO4·2H2O)的生产流程示意图:
石膏(CaSO4·2H2O)的生产流程示意图: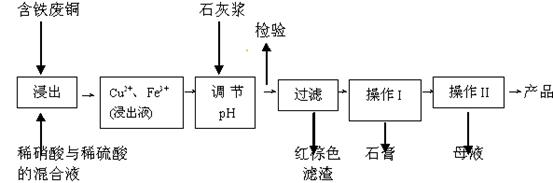
温度(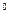 C) C) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
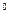 C左右;
C左右;科目:高中化学 来源:不详 题型:填空题
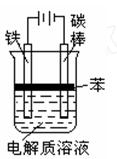
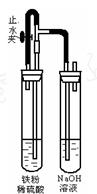
| A.氯化钠溶液 | B.稀硫酸 | C.硫酸铜溶液 | D.碳酸钠溶液 |
 。
。 右侧试管内可见到白色沉淀。
右侧试管内可见到白色沉淀。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 6SO2+Fe3O4,若有3 mol FeS2参加反应,则转移 mol电子。
6SO2+Fe3O4,若有3 mol FeS2参加反应,则转移 mol电子。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(m-2.4)g | B.(m-1.6) g | C.(m-3.2)g | D.无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com