
现有稀硫酸和稀硝酸的混合溶液,已知其中稀硫酸浓度为4mol/L,稀硝酸的浓度为2mol/L。取10mL混合酸,向其中加入过量铁粉,反应结束后,在标准状况下可收集到气体体积为(假设HNO3只被还原为NO)( )
A.0.224L B.0.448L C.0.672L D.0.896L
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
如图所示是在航天用高压氢镍电池基础上发展起来的一种金属氢化物镍电池(MHNi电池)。下列有关说法不正确的是( )
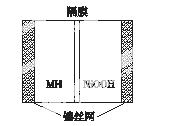
A.放电时正极反应为NiOOH+H2O+e-—→Ni(OH)2+OH-
B.电池的电解液可为KOH溶液
C.充电时负极反应为MH+OH-—→H2O+M+e-
D.MH是一类储氢材料,其氢密度越大,电池的能量密度越高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与化学反应 能量变化相关的叙述正确的是( )
能量变化相关的叙述正确的是( )
A.反应热就是反应放出的热量
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应热
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素周期表和元素性质的说法中正确的是( )
A.除短周期外,其他周期均有32种元素
B.同一主族元素的原子,最外层电子数相同,化学性质完全相同
C.副族元素中没有非金属元素
D.非金属元素只能形成共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
元素W、X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为34,M原子的最外层电子数与次外层电子数之比为34,且M原子的质子数是Y原子的2倍;X元素的最高正价与最低负价绝对值之差为2;N-、Z+、W+的半径逐渐减小;化合物WN常温下为气体,据此回答下列问题:
(1)W与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式:
___________________________________________________________。
(2)下图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:_________。
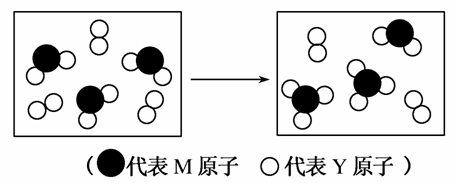
(3)A、B均为由上述六种元素中的三种元素组成的强电解质,且组成元素的原子个数之比均为1:1:1。若在各自的水溶液中,A能抑制水的电离,B能促进水的电离,则A的化学式为________,B的电子式是________。
(4)如对盛有气体XY2的密闭容器(带可移动的活塞)进行压缩操作,产生的现象是_________________________________________,原因是______
_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)=== NH4Cl(s)在室温下可自发进行,则该反应的△H>0
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
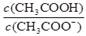 C.CH3COOH 溶液加水稀释后,溶液中 的值减小
C.CH3COOH 溶液加水稀释后,溶液中 的值减小
D.Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示,据图分析,下列判断错误的是( )
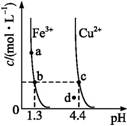
A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
B.加适量NH4Cl固体可使溶液由a点变到b点
C.c、d两点代表的溶液中c(H+)与c(OH-)乘积相等
D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
查看答案和解析>>
科目:高中化学 来源: 题型:
关于某有机物 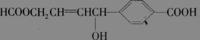 的性质叙述正确的是 ( )
的性质叙述正确的是 ( )
A、1 mol该有机物可以与3 mol Na发生反应、
B、1 mol该有机物可以与3 mol NaOH发生反应
C、1 mol该有机物可以与6 mol H2发生加成反应
D、1 mol该有机物分别与足量Na或NaHCO3反应,产生的气体在相同条件下体积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述与图像对应符合的是( )
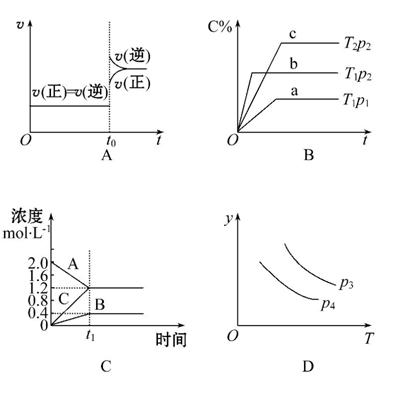
A.对于达到平衡状态的N2(g)+3H2(g)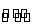 2NH3(g)在t0时刻充入了一定的NH3,平衡逆向移动
2NH3(g)在t0时刻充入了一定的NH3,平衡逆向移动
B.p2>p1,T1>T2
C.该图像表示的方程式为:2A====B+3C
D.对于反应2X(g)+3Y(g)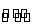 2Z(g) ΔH<0,y可以表示Y的百分含量
2Z(g) ΔH<0,y可以表示Y的百分含量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com