
分析 (1)配制250mL Na2SO3溶液时,用到的实验仪器有:烧杯、玻棒、胶头滴管、药匙、天平、250mL容量瓶;
(2)Na2SO3固体氧化变质生成硫酸钠;
(3)方案I是利用生成的硫酸钡沉淀计算样品中硫酸钠的质量,再计算亚硫酸钠的纯度,而亚硫酸钠也会与氯化钡反应生成沉淀,影响硫酸钡质量的测定,需要出去亚硫酸钠;
SO42-完全沉淀时,上清液没有SO42-,再加入氯化钡溶液也没有沉淀生成;
(4)方案I中,若滤液浑浊,说明滤液中含有硫酸钡,导致沉淀硫酸钡的质量偏小,计算样品中硫酸钠的质量偏小;
(5)酸性条件下,硝酸根将亚硫酸根氧化为硫酸根,导致硫酸钡质量增大;
(6)V-消耗KMnO4溶液体积为 V mL,KMnO4溶液浓度为c mol/L,计算高锰酸钾的物质的量,根据电子转移守恒计算Na2SO3的物质的量,进而计算样品的纯度.
解答 解:(1)用天平称量固体质量,用到药匙,在烧杯中溶解,并用玻璃棒搅拌,用玻璃棒引流移入250mL容量瓶中,加水至刻度线1-2cm出改用胶头滴管定容,
故答案为:天平、250mL容量瓶;
(2)Na2SO3固体氧化变质生成硫酸钠,反应方程式为:2Na2SO3+O2=2Na2SO4 ,
故答案为:2Na2SO3+O2=2Na2SO4 ;
(3)方案I是利用生成的硫酸钡沉淀计算样品中硫酸钠的质量,再计算亚硫酸钠的纯度,而亚硫酸钠也会与氯化钡反应生成沉淀,影响硫酸钡质量的测定,需要出去亚硫酸钠,加入过量的盐酸酸化的BaCl2溶液,目的是:使SO32-充分转化为气体,在过滤前,需要检验是否沉淀完全,其操作是:静置,在上层清液中再滴入氯化钡溶液,观察是否继续有沉淀生成,
故答案为:使SO32-充分转化为气体;静置,在上层清液中再滴入氯化钡溶液,观察是否继续有沉淀生成;
(4)方案I中,若滤液浑浊,说明滤液中含有硫酸钡,导致沉淀硫酸钡的质量偏小,计算样品中硫酸钠的质量偏小,则计算亚硫酸钠的质量分数偏高,
故答案为:偏高;
(5)方案II中盐酸提供H+,Ba(NO3)2提供NO3-形成稀HNO3,将一部分SO32-氧化成SO42-,导致BaSO4质量增大,
故答案为:<;方案II中盐酸提供H+,Ba(NO3)2提供NO3-形成稀HNO3,将一部分SO32-氧化成SO42-,导致BaSO4质量增大;
(6)V-消耗KMnO4溶液体积为 V mL,KMnO4溶液浓度为c mol/L,
则消耗高锰酸钾的物质的量为0.001V L×c mol/L=0.001Vc mol,根据电子转移守恒,Na2SO3的物质的量为0.001Vc mol×$\frac{5}{2}$=0.002.5Vc mol,其质量为0.002.5Vc mol×126g/mol=0.315Vc g,故250mL溶液中亚硫酸质量为0.315Vc g×$\frac{250mL}{25mL}$=3.15Vc g,则样品中亚硫酸钠的质量为$\frac{3.15Vc}{W}$×100%,
故答案为:$\frac{3.15Vc}{W}$×100%(V-KMnO4溶液体积--mL,c-KMnO4溶液浓度--mol/L).
点评 本题考查物质含量测定实验,(6)中表达式为易错点,需要学生理解氧化还原反应滴定原理,题目侧重对实验原理与误差的分析,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 CH3COOH溶液与0.1 mol•L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)>c(CH3COO-) | |
| B. | 10 mL 0.1 mol•L-1 CH3COONa溶液与10 mL 0.1 mol•L-1 CH3COOH溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 0.1 mol•L-1 NaHCO3溶液与0.1 mol•L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 待提纯的物质 | 选用的试剂 |
| A | N2(O2) | 灼热的铜网 |
| B | SO2(SO3) | 饱和Na2SO3溶液 |
| C | H2(H2S) | CuSO4溶液 |
| D | CO2(SO2) | 酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

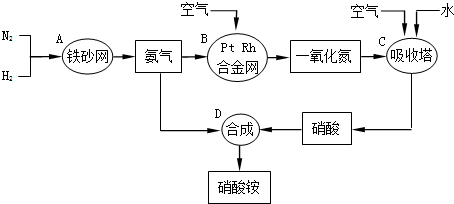
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4和SiCl4的熔点 | |
| B. | 邻羟基苯甲醛( )和对羟基苯甲醛( )和对羟基苯甲醛(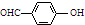 )的沸点 )的沸点 | |
| C. | HF和HCl在水中的溶解度 | |
| D. | H2SO3和H2SO4的酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com