
水热法制备Fe3O4纳米级颗粒的反应为3Fe2+ +2S2O32-+O2 +xOH-=Fe3O4+S4O62-+2H2O,下列说法中,不正确的是
A.每生成1mol Fe3O4,反应转移的电子总数为4mol
B.Fe2+和S2O32-都是还原剂
C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol
D.x=4
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届河北省高三上学期四调考试化学试卷(解析版) 题型:填空题
(8分)W、X、Y、Z四种短周期元素在周期表中的位置如图所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物。


请回答下列问题。
(1)H2Y2的电子式为______________________,Z在周期表中的位置___________________。
(2)在图中,b的pH约为7,且含有Fe2+和淀粉KI的水溶液,a为H2Y2的水溶液,旋开分液漏斗旋钮,观察到烧瓶中溶液呈蓝色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是_________________________。
(3)已知:298K时,金属钠与Y2气体反应,若生成1molNa2Y固体时,放出热量414kJ;若生成1molNa2Y2固体时,放出热量511kJ。则由Na2Y固体与Y2气体反应生成Na2Y2固体的热化学方程式为_____________。
(4)有人设想利用原电池原理以气体Z2和氢气制备一种重要的化工原料,同时获取电能。假设这种想法可行,用石墨作电极材料,用稀盐酸作电解溶液,则通入Z2的电极为原电池的___________极,其电极反应式为____________________。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春市高三上学期期中测试化学试卷(解析版) 题型:选择题
已知下列反应: 反应Ⅰ:Co2O3 + 6HCl(浓)= 2CoCl2 + Cl2↑+ 3H2O
反应Ⅱ:5Cl2 + I2 + 6H2O = 10HCl + 2HIO3 下列说法正确的是
A.反应Ⅰ中HCl是氧化剂 B.反应Ⅱ中Cl2发生氧化反应
C.还原性:CoCl2 > HCl > I2 D.氧化性:Co2O3 > Cl2 >HIO3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃兰州一中高二上期中测试理科化学试卷(解析版) 题型:填空题
(8分)t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12。
(1)该温度下,水的离子积常数Kw= 。
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH= ,此时该溶液中由水电离的c(OH-)= 。
(3)该温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃兰州一中高二上期中测试文科化学试卷(解析版) 题型:填空题
(1)(8分)从能量角度看,断开化学键要 ,形成化学键要 ,一个化学反应是释放能量还是吸收能量取决于 ;水的分解需要吸收热量,试从化学键变化的角度分析原因 。
(2)(2分)4克硫粉完全燃烧时放出37kJ热量,该反应的热化学方程式是: 。
(3)(10分)现在下列物质:①100℃的纯水;②25℃0.1mol/LHCl溶液;③25℃0.1mol/LKOH溶液;④25℃0.1mol/LBa(OH)2溶液。
这些物质与25℃纯水相比,能促进水的电离的是 (填序号,以下同);
能抑制水的电离的是 ;
水电离的c(OH-)水等于溶液中c(OH-)的是 ;
水电离的c(H+)水等于溶液中c(H+)的是 ;
以上可得出一个结论,纯水中加入酸、碱,可 水的电离(填促进、抑制、不影响)
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三上学期第二次月考理综化学试卷(解析版) 题型:推断题
(14分)已知D、M、H是常见得非金属单质,其中M是无色气体,H是有色气体。J是一种金属单质(其同族的某种元素是形成化合物种类最多的元素),A、C是金属氧化物,C和J均是某种常见电池的电极材料,J元素的+2价化合物比+4价化合物稳定,B与C反应时,每生成1molH同时消耗4molB和1molC。K只知含有CO或CO2中的一种或两种。它们关系如下图所示:
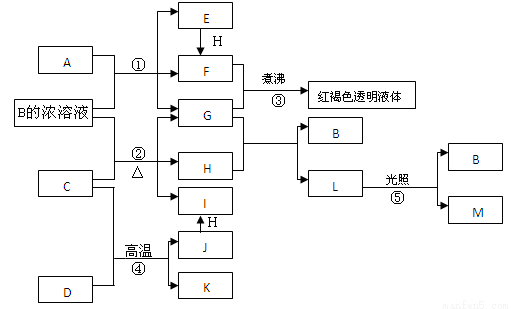
(1)写出A物质中所含金属元素在周期表中的位置:_________________。
(2)写出化合物L的电子式:______________ 反应②的化学方程式为_________________。
(3)向图中的红褐色透明液体中逐滴滴入HI溶液,可以观察到先产生红褐色沉淀,后红褐色沉淀溶解,红褐色沉淀溶解的离子方程式为_______________。
(4)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用_______________(填序号)方法
①热还原法 ②电解法 ③热分解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为________mol。
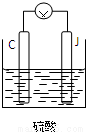
(5)用C、J作电极,与硫酸构成如图所示原电池,负极的电极反应为__________,当反应转移2mol电子时,负极质量增加______克。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南外国语学校高三上学期期中测试化学试卷(解析版) 题型:选择题
甲、乙两烧杯中分盛有10mL1mol•L-1AlCl3溶液,在甲烧杯中加入一定量NaOH溶液;乙烧杯中加入与上述NaOH溶液等体积、等pH的氨水.下列有关两个烧杯的说法中,正确的是
A.甲中产生的沉淀一定比乙中多 B.乙中产生的沉淀一定比甲中多
C.甲和乙产生的沉淀一定一样多 D.甲和乙中产生的沉淀可能一样多
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南洛阳高级中学高二上9月月考化学试卷(解析版) 题型:选择题
室温下,将1 mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1 mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为CuSO4·5H2O(s)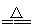 CuSO4(s)+5H2O(l),热效应为ΔH3,则下列判断正确的是
CuSO4(s)+5H2O(l),热效应为ΔH3,则下列判断正确的是
A.ΔH2>ΔH3 B.ΔH1+ΔH3=ΔH2
C.ΔH1<ΔH3 D.ΔH1+ΔH2>ΔH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
已知2CO(g)+O2(g)═2CO2(g)△H=-566kJ/mol
Na2O2(s)+CO2(g)═Na2CO3(s)+1\2O2(g)△H=-266kJ/mol
根据以上热化学方程式,下列判断正确的是
A.CO的燃烧热为283kJ
B.2molCO2(g)与2molNa2O2(s)反应放出452kJ热量时,电子转移数约为1.204×1024
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H<-452kJ/mol
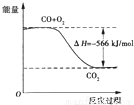
D.如图可表示CO生成CO2,的反应过程和能量关系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com