
【题目】某校化学兴趣小组用如下装置图验证NO2的氧化性和NO的还原性。请回答下列问题:

(1)写出甲中反应的离子方程式:______________;
(2)说明NO2具有氧化性的现象是_________________;
(3)说明NO具有还原性的操作和现象是______________;
(4)小组一成员对实验设计提出了质疑,他认为乙中的现象不足以证明NO2的氧化性,他的理由除了硝酸具有挥发性外,还有可能是_____________________________________;经小组讨论,他们设计了以下方案,其中合理的是__________
A.NO2与HCl气体混合 B.NO2与H2S气体混合 C.NO2通入Na2S溶液中
【答案】 Cu + 4H+ + 2NO3- = Cu2+ + NO2↑ + 2H2O 淀粉KI溶液变蓝 打开开关,挤压气囊;丙中气体由无色变为红色 NO2和水反应生成的HNO3是一种氧化性酸,也可将I-氧化成I2,使溶液变蓝 B
【解析】(1)铜和浓硝酸反应生成硝酸铜、二氧化氮和水,离子反应方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;(2)NO2具有氧化性,能将碘离子氧化为单质碘,碘单质遇到淀粉变蓝色,所以乙试管中溶液变蓝色可以证明NO2具有氧化性;(3)二氧化氮和水反应生成的一氧化氮和氧气反应生成红棕色气体二氧化氮,说明NO具有还原性,所以看到的现象是:有红棕色气体生成;(4)二氧化氮和水反应生成硝酸,硝酸具有强氧化性,所以硝酸也能把碘离子氧化生成碘单质,对二氧化氮性质的检验造成干扰;为防止硝酸的干扰,故应在无水的环境中检验NO2的氧化性,将干燥的NO2与干燥的H2S气体混合,若有淡黄色固体生成,即可证明NO2的氧化性,答案选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某工厂用 FeCl3 溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL 废液加入足量的 AgNO3 溶液,生成沉淀 8.61g。(2)另取 10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液组成的判断错误的是
A. 一定含有 Fe 2+、 Fe 3+、 Cu2+、 Clˉ B. c(Fe2+):c(Cu2+) = 2:1
C. c(Clˉ) = 6mol / L, c(Fe 2+) = 1.2mol / L D. c (Fe2+):c(Fe 3+) = 3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于物质的类别,下列说法正确的是
A.食盐水、糖水、冰水都属于混合物
B.烧碱、火碱、消石灰都属于碱
C.KHSO4、HCl、HNO3在水中都能电离出氢离子,都属于酸
D.溶液、胶体、浊液都属于稳定的分散系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向18.4g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成NO2、NO混合气体,再向所得溶液中加入足量的NaOH溶液,生成30.3g沉淀.另取等质量的合金,使其与一定量的氯气恰好完全反应,则氯气的体积在标准状况下为
A.7.84L B.6.72L C.4.48L D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸钠(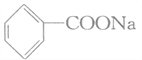 ,缩写为NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A-,已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.7×10-7,Ka2=4.90×10-11,在生产碳酸饮料的过程中除了添加NaA外,还需加压充入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)
,缩写为NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A-,已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.7×10-7,Ka2=4.90×10-11,在生产碳酸饮料的过程中除了添加NaA外,还需加压充入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)
A. 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B. 提高CO2充气压力,饮料中c(A-)不变
C. 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO3-)+c(CO32-)+c(OH-)-c(HA)
D. 当pH为5.0时,饮料中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的三种盐 NaX、NaY和NaZ的溶液,若它们的pH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的排列顺序是 ( )
A.HX、HZ、HY B.HZ、HY、HX C.HX、HY、HZ D.HY、HZ、HX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知碘(I)元素有﹣1、+l、+3、+5、+7等多种化合价,有些碘的氧化物可以看成是由带正电荷的碘离子和碘酸根离子(IO3﹣)构成.下列的化学式是碘酸碘的是( )
A.I2O5
B.I2O4
C.I4O5
D.I4O9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中CH3COO-和Na+浓度相等,则醋酸体积__________氢氧化钠溶液体积 (填“>”“=”“<”)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液,溶液中c(Na+)___________c(CH3COO-)(填“>”“=”“<”)。
(3)某温度(t℃)时,水的KW=10-13,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4的溶液bL混合,若所得混合液为中性,则a∶b___________;若所得混合液的pH=2,则a∶b___________。
(4)室温下,若某pH值的硫酸溶液中水电离的c(H+)=1.0×10-amol·L-1,而相同pH值的硫酸铝溶液中水电离出的c(H+)=1.0×10-b mol·L-1,(已知a.b均小于14的正整数),那么a和b之间满足的数量关系是____________(用一个等式和一个不等式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 反应KClO3+6HCl=3Cl2+KCl+3H2O,每生成1.5molCl2转移电子数为2.5NA
B. 标准状况下,11.2LNO与11.2LO2混合后所含分子数为0.75NA
C. 1L 0.1 molL-1NH4Cl溶液中NH4+的数目为0.1NA
D. 40gSiC中含有Si—C键的数目为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com