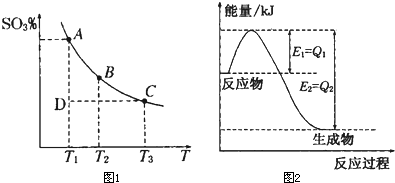
运用化学反应原理研究碳的氧化物的性质具有重要意义.
(1)CO
2是一种重要的物质,但其过量排放,可能导致全球气温升高.下列措施不能够有效控制CO
2所导致的温室效应的是
④
④
(填序号)
①大力发展低碳产业,提倡低碳生活,依法控制CO
2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数K
a1=4.2×10
-7,K
a2=5.6×10
-11;次氯酸在水中的电离常数K
a=4.7×10
-8.写出84消毒液露置在空气中发生反应的离子方程式
ClO-+CO2+H2O=HClO+HCO3-;2HClO=2H++2Cl-+O2↑
ClO-+CO2+H2O=HClO+HCO3-;2HClO=2H++2Cl-+O2↑
.
(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na
2O
2反应.
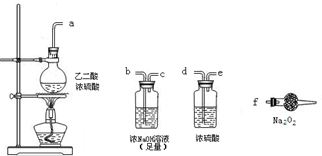
已知:H
2C
2O
4 CO
2↑+CO↑+H
2O,则实验选择的最简单的装置接口连接顺序为
abcf
abcf
;若CO能够与Na
2O
2发生反应,则预测反应产物为
Na2CO3
Na2CO3
.
(4)已知C(s)+O
2(g)=CO
2(g),△H=-393.5kJ?mol
-1;CO(g)+
O
2(g)=CO
2(g),△H=-283.0kJ?mol
-1,写出CO
2 和C(s)反应的热化学方程式
CO2(g)+C(s)=2CO(g)△H=+172.5kJ?mol-1
CO2(g)+C(s)=2CO(g)△H=+172.5kJ?mol-1
.以CO为燃料制作燃料电池,电池的正极通入O
2和CO
2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为
CO+CO32-→2CO2+2e-
CO+CO32-→2CO2+2e-
.若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)
11.2
11.2
L.




 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
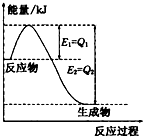 运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.