
| A.SO2中S原子含1对孤电子对 | B.BeCl2是直线形分子 |
| C.SO3的空间构型为平面三角形 | D.H20的VSEPR构型和空间构型都是V形 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
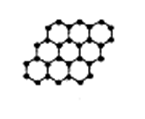
| A.石墨烯与石墨互为同位素 |
| B.0.12g石墨烯中含6.02×l022个碳原子 |
| C.石墨烯是一种化合物 |
| D.在整个单层片结构中属于每个六边形的碳原子数实际为2个 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
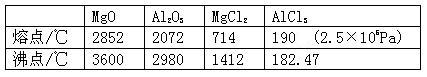
 (2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是__ _____。
(2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是__ _____。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素的非金属性越强,其单质的活泼性一定越强 |
| B.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性 |
| C.分子晶体的熔沸点低,常温下均呈液态或气态 |
| D.含有金属阳离子的晶体一定是离子晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 .0g。通过计算请回答下列问题(请写出计算过程)。
.0g。通过计算请回答下列问题(请写出计算过程)。 的气体体积;
的气体体积; 2)开始析出MgSO4·xH2O晶体时溶液的质量分数;
2)开始析出MgSO4·xH2O晶体时溶液的质量分数;查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B.熔点由高到低: Na>Mg>Al |
| C.硬度由大到小: 金刚石>碳化硅>晶体硅 |
| D.结合质子能力:OH->CH3COO->Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2个O2-相紧邻
2个O2-相紧邻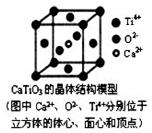
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com