

| ���� | ��Է������� | ��״ | �۵� | �е� | �ܶ� | �ܽ�� | ||
| ˮ | �Ҵ� | ���� | ||||||
| �ױ� | 92 | ��ɫҺ����ȼ�ӷ� | -95 | 110.6 | 0.8669 | ���� | ���� | ���� |
| ������ | 122 | ��ɫƬ״����״���� | 122.4 | 248 | 1.2659 | �� | ���� | ���� |
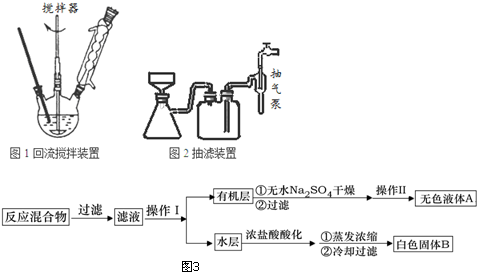
 ������������
��������Ϊ�������� һ�����ļױ���������KMnO4��Һ��100�淴Ӧһ��ʱ���ֹͣ��Ӧ������ͼ���̷����������ͻ���δ��Ӧ�ļױ���������������ˮ���ױ�������ˮ���������ܵ�Һ����÷�Һ�������룬����ʵ��Ŀ��֪���Ӷ��õ��л����ˮ�㣬�л����к��мױ���ˮ���к��б����ᣬ�л����еļױ����������õ���ɫҺ��A��A�Ǽױ�����ˮ�������ữ������Ũ�������ݱ�������ܽ��֪���õ��Ĺ���B�DZ����ᣬ
��1��A�Ǽױ������뻥���ҷе㲻ͬ��Һ�����������
��2�������Һ����ɫ��˵��������ع�����Ҫ�ȼ���������أ���������ػ�ԭ������Ũ������ܱ�������������
��3��A������ʱ��ƿ��ѹǿ��С�����Լӿ�����ٶȣ�
B��Ϊ�˷�ֹ������¶˴�������ƿ���¶ȼƣ���˲��������ǽӴ���
C��ͼ1��������װ��Ӧ����ˮԡ���ȵķ�����
D����������ˮ�������������������෴��
��4���ױ���NaOH����Ӧ����������NaOH��Ӧ���ɱ������ƣ���Һ������������Һ�м���������Ƶñ����
��5���������KOH��Һ��������кͷ�Ӧ�����ݱ������KOH֮��Ĺ�ϵʽ���㱽������������Ӷ����㱽���������������
��� �⣺һ�����ļױ���������KMnO4��Һ��100�淴Ӧһ��ʱ���ֹͣ��Ӧ������ͼ���̷����������ͻ���δ��Ӧ�ļױ���������������ˮ���ױ�������ˮ���������ܵ�Һ����÷�Һ�������룬����ʵ��Ŀ��֪���Ӷ��õ��л����ˮ�㣬�л����к��мױ���ˮ���к��б����ᣬ�л����еļױ����������õ���ɫҺ��A��A�Ǽױ�����ˮ�������ữ������Ũ�������ݱ�������ܽ��֪���õ��Ĺ���B�DZ����ᣬ
��1��A�Ǽױ�����ṹ��ʽΪ ���л��������ʻ����ҷе㲻ͬ�����Կ��Բ����������룬�����IIΪ����
���л��������ʻ����ҷе㲻ͬ�����Կ��Բ����������룬�����IIΪ����
�ʴ�Ϊ�� ������
������
��2�������Һ����ɫ��˵��������ع�����Ҫ�ȼ���������أ���ȥδ��Ӧ�ĸ�����أ�����Ũ�����ữʱ���ܱ��������������������
�ʴ�Ϊ����ȥδ��Ӧ�ĸ�������������������������ữʱ�ᷢ�����ᱻ�������������������������
��3��A������ʱ��ƿ��ѹǿ��С�����Լӿ�����ٶȣ��õ��ϸ���ij�������A��ȷ��
B��Ϊ�˷�ֹ������¶˴�������ƿ���¶ȼƣ���˲��������ǽӴ��������ڽ���ʱ��������¶˲�����������ƿ�ס��¶ȼƵȽӴ�����B��ȷ��
C����ˮԡ���ȱ��ڿ����¶Ⱥ�ʹ�������Ⱦ��ȣ�ͼ1��������װ��Ӧ����ˮԡ���ȵķ�������C����
D����������ˮ�������������������෴������������ˮ���������½��ϳ�����D��ȷ��
�ʴ�Ϊ��ABD��
��4����ȥ�����ڱ������еļױ�Ӧ�ȼ��룬Ӧ���ȼ�NaOH��Һ���ױ���NaOH����Ӧ����������NaOH��Ӧ���ɱ������ƣ���Һ������������Һ�м���������Ƶñ����ᣬ
�ʴ�Ϊ��NaOH��Һ��Ũ�����ữ��
��5���豽��������ʵ���Ũ��Ϊx����25mL��������Һ�б���������ʵ���Ϊ0.025xmol��
C6H5COOH+KOH��C6H5COOK+H2O
1mol 1mol
0.025xmol 2.40��10-3mol
1mol��1mol=0.025xmol��2.40��10-3mol
x=$\frac{2.4��1{0}^{-3}mol��1mol}{1mol��0.025mol}$=0.96��
��100mL����������������=0.096mol/L��0.1L��122g/mol=1.1712g������������=$\frac{1.1712g}{1.220g}$=96%��
�ʴ�Ϊ��96%��
���� ���⿼����ʵ�鷽����ơ������ķ�����ᴿ�����ؿ����������������������������ȷ���ʵ������ǽⱾ��ؼ���֪���������ʵ�����ѡȡ���ʵķ��뷽������Ŀ�Ѷ��еȣ�


 �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д� ����ѧ��Ӯ�����ϵ�д�
����ѧ��Ӯ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���������ɫ���壬������ͨ��Μ[ʯ��ˮ����Һ����ǣ�һ����CO32- | |
| B�� | �����Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��һ����SO42- | |
| C�� | ����KSCN��Һ�����������ټ���������ˮ��Һ��ΪѪ��ɫ��һ����Fe2+ | |
| D�� | ���������������Һ��������ɫ�������ټ���ϡ����������ܽ⣬��һ������C1- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H1-��H2 | B�� | ��H2-��H1 | C�� | ��H1+��H2 | D�� | 2��H1-2��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25��ʱ��0.1 mol/LHX��Һ��pH=1 | |
| B�� | Ksp��CaX2�����¶Ⱥ�Ũ�ȵı仯���仯 | |
| C�� | ����ϵ�У�c��Cl-��=c��Ca2+�� | |
| D�� | ����ϵ��HX��CaCl2��Ӧ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�s2�s3 | B�� | 1�s1�s1 | C�� | 2�s3�s6 | D�� | 3�s2�s1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
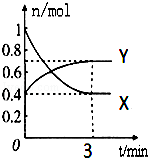 ��һ���¶��£����Ϊ2L���ܱ������У�NO2��N2O4֮�䷢����Ӧ��2NO2��g��������ɫ��?N2O4g������ɫ������ͼ��ʾ��
��һ���¶��£����Ϊ2L���ܱ������У�NO2��N2O4֮�䷢����Ӧ��2NO2��g��������ɫ��?N2O4g������ɫ������ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
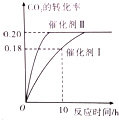 ��֪CO2��������ɫȼ�ϼ״���CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H��0 300��ʱ�ܱ������У���c��CO2��=1.00mol/L��c��H2��=1.60mol/L��ʼ��Ӧ�������ͼ��ʾ���ش��������⣺
��֪CO2��������ɫȼ�ϼ״���CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H��0 300��ʱ�ܱ������У���c��CO2��=1.00mol/L��c��H2��=1.60mol/L��ʼ��Ӧ�������ͼ��ʾ���ش��������⣺�鿴�𰸺ͽ���>>
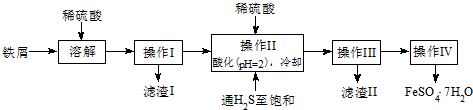
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| 25��ʱ | pHֵ |
| ����H2S��Һ | 3.9 |
| SnS������ȫ | 1.6 |
| FeS��ʼ���� | 3.0 |
| FeS������ȫ | 5.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com