
【题目】下列铜原子核外电子排布式正确的是( )
A.1s22s22p63s23p64s2B.1s22s22p63s23p64s1
C.1s22s22p63s23p63d104s1D.1s22s22p63s23p63d94s2
科目:高中化学 来源: 题型:
【题目】用无机矿物资源生产部分材料,其产品流程示意图如下。下列有关说法错误的是

A. 制取玻璃和粗硅时生成的气体产物均为CO2
B. 生产铝、铜及高纯硅的过程中都涉及氧化还原反应
C. 粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法
D. 黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列制取硫酸铜的实验设计中,能体现“经济、高效、环保”精神的最佳方案是( )。
A. 铜与浓硫酸共热
B. 用铜片为阳极,石墨为阴极,电解稀硫酸
C. 先灼烧废铜屑生成氧化铜,然后再用浓硫酸溶解
D. 适当温度下,使铜片在持续通入空气的稀硫酸中溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值,下列说法中,正确的是( )
A. 标准状况下,22.4L Cl2完全溶于水时,转移的电子数为NA
B. 16g甲基中含有的质子数目为10NA
C. 标准状况下,2.24L NH3中含有的共价键数目为NA
D. 常温下,23g NO2和N2O4的混合气体中含有NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:
CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积均为2L的三个恒温密闭容器中,加入一定量的反应物发生反应.相关数据如下:
容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系 能量的变化 | |||
n(CO) | n(H2O) | n(CO2) | n(H2) | ||
① | 1 | 4 | 0 | 0 | 放出热量:32.8 kJ |
② | 0 | 0 | 1 | 4 | 热量变化:Q1 |
③ | 1 | 1 | 2 | 1 | 热量变化:Q2 |
下列说法中,不正确的是( )
A. 若容器①中反应10min达到平衡,0至10min时间内,用CO表示的平均反应速率υ(CO)= 4.0×10﹣2 mol/(L·min)
B. 容器③中,开始时υ(CO)生成>υ(CO)消耗
C. 达平衡过程体系能量的变化:Q1= 4Q2
D. 平衡时,①与②容器中CO的体积分数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 鸡蛋壳浸泡在盐酸中产生气泡:CO![]() +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
B. 小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O
C. 碘化亚铁溶液中通入少量Cl2:Cl2+2I-===2Cl-+I2
D. 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4- + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在水溶液中1molCl-,ClOx(x=1,2,3,4)的能量(kJ)相对大小如图所示.下列有关说法正确的是( )
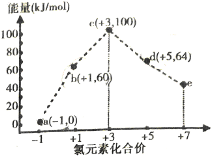
A.e是ClO3-
B.b→a+c反应的活化能为60kJmol-1
C.a,b,c,d,e中c最稳定
D.b→a+d反应的热化学方程式为3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-116kJmol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com