
下列离子组能大量共存的是
A.Cu2+、Na+、OH- B.H+、Cl-、CH3COO-
C.Fe3+、H+、NO3- D.K+、Ca2+、CO32-
科目:高中化学 来源:2015届江苏省教学协作体高二上学期期末化学试卷(解析版) 题型:选择题
下列变化过程中,不涉及化学变化的是
A.碳的燃烧 B.水的通电分解
C.钢铁融化制铁锅 D.氨气溶于水
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二上学期期末考试化学试卷(选修)(解析版) 题型:选择题
“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e- = X + 2H+。下列说法中正确的是
A.电池内部H+由正极向负极移动
B.另一极的电极反应式为:O2 + 4e- + 2H2O = 4OH-
C.乙醇在正极发生反应,电子经过外电路流向负极
D.电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二上学期期末考试化学试卷(必修)(解析版) 题型:选择题
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如下图。下列有关该氢氧燃料电池的说法错误的是
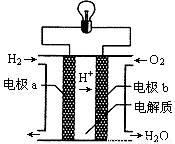
A.该电池工作时将化学能转化为电能
B.电流从电极b经外电路流向电极a
C.该电池中的电极b是正极
D.在电极a上发生还原反应
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二上学期期末考试化学试卷(必修)(解析版) 题型:选择题
在汽车尾气处理装置中常发生如下反应:4CO+2NO2=4CO2+N2。下列对该反应的说法中正确的是
A.该反应属于置换反应
B.该反应中氧化剂是CO,还原剂是NO2
C.该反应生成14 g N2时,转移8 mol e-
D.该反应能减少汽车尾气对环境的污染
查看答案和解析>>
科目:高中化学 来源:2015届江苏省扬州市高二上学期期末考试化学试卷(必修)(解析版) 题型:选择题
将秸秆、粪便等转化为沼气,既可获得清洁能源又可改善环境质量。沼气的主要成分是
A.CO B.CH4 C.H2 D.H2S
查看答案和解析>>
科目:高中化学 来源:2015届山西省大同市高二上学期期末考试化学试卷(解析版) 题型:选择题
以溴乙烷为原料制备1,2?二溴乙烷,下列方案中最合理的是( )
A.CH3CH2Br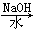 CH3CH2OH
CH3CH2OH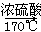 CH2=CH2
CH2=CH2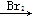 CH2BrCH2Br
CH2BrCH2Br
B.CH3CH2Br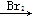 CH2BrCH2Br
CH2BrCH2Br
C.CH3CH2Br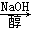 CH2=CH2
CH2=CH2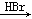 CH2BrCH3
CH2BrCH3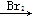 CH2BrCH2Br
CH2BrCH2Br
D.CH3CH2Br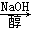 CH2=CH2
CH2=CH2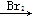 CH2BrCH2Br
CH2BrCH2Br
查看答案和解析>>
科目:高中化学 来源:2015届山东省济宁市高二3月质检化学试卷(解析版) 题型:实验题
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。
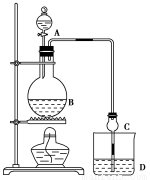
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/ ℃ | 34.7 | 78.5 | 118 | 77.1 |
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)浓硫酸的作用是 ;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式: 。
球形干燥管C的作用是 。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是(用离子方程式表示) ;反应结束后D中的现象是 。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出 。
查看答案和解析>>
科目:高中化学 来源:2015届天津市红桥区高二上学期期末考试化学试卷(解析版) 题型:选择题
在一体积为10 L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)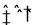 CO2(g)+H2(g) △H<0。
CO2(g)+H2(g) △H<0。
(1)CO和H2O浓度变化如图,则在该温度下,该反应的平衡常数K= 。
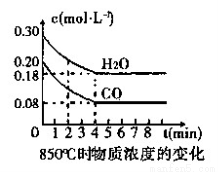
0~4 min的平均反应速率v(CO)= mol·L-1·min-1。若降低温度,该反应的K值将 ,该反应的化学反应速率将 (填“增大”“减小”或“不变”)。
(2)在相同容器中发生上述反应,当温度高于850℃时,容器内各物质的浓度变化如下表。
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 |
|
6 | 0.096 | 0.266 | 0.104 |
|
①表中3 min~4 min之间反应处于 状态;cl数值 0.08 mol·L-1(填大于、小于或等于)。
②反应在4 min~5 min之间,平衡向逆方向移动,可能的原因是
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
(3)在相同温度下(850℃),若起始时c(CO)=1mol·L-1,C(H2O)=2mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com