
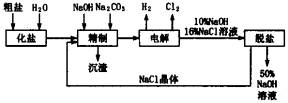
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上发生反应的化学方程式为____________,与电源负极相连的电极附近,溶液Ph________(选填“不变”“升高”或“下降”)。
(2)工业食盐含Ca2+、Mg2+、SO42-等杂质。精制过程发生反应的离子方程式为________。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去________,该钡试剂可以是________。
(选填“a”“b”或“c”,多选扣分)
A. Ba(OH)2 B. Ba(NO3)2 C. BaCl2
(4)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为____________。
(选填“a”“b”或“c”,多选扣分)
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、_______
除去NaCl。(填写操作名称)
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应,采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________
| 点拨解答:本题是对电解原理在氯碱工业上实际运用的高度浓缩。从尿料的精制、电解原理的运用、除杂试剂的选取和使用顺序、NaOH和NaCl的分离等方面全面人手,完整地反映出氯碱工业中各种产品的生产过程,深入分析了在生产过程中可能出现的副反应。充分反映了理论对实际生产的指导意义,对我们学习和理解电解原理起到了深化、巩固、提高的作用。与电源正极相连的是阳极发生氧化反应,CI-放电,阴极水电离产生的H+放电,OH-的浓度增大,故:
(1)2Cl--2e-=Cl2↑升高 (2)Ca2++CO32-=CaCO3↓ Mg2++2OH-=Mg(OH)2+↓ (3)a c (4)b c (5)蒸发 过滤 (6)NaCl+H2O=NaCIO+H2↑(或2NaCI+2H2O=H2 ↑+Cl2↑+2NaOH、Cl2+2NaOH=NaCl+NaClO+H2O)
|


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A.2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
B.H2+Cl2![]() 2HCl
2HCl
C.Cl2+2NaOH![]() NaClO+NaCl+H2O
NaClO+NaCl+H2O
D.Cl2+H2O![]() HCl+HClO
HCl+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
A.2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
B.H2+Cl2![]() 2HCl
2HCl
C.Cl2+2NaOH![]() NaCl+NaClO+H2O
NaCl+NaClO+H2O
D.Cl2+H2O![]() HCl+HClO
HCl+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
A.2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑?
2NaOH+H2↑+Cl2↑?
B.H2+Cl2![]() 2HCl?
2HCl?
C.Cl2+2NaOH![]() NaClO+NaCl+H2O?
NaClO+NaCl+H2O?
D.Cl2+H2O![]() HCl+HClO
HCl+HClO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com