
| A. | 1.2×10-3mol•L-1 | B. | 1.2×10-9mol•L-1 | C. | 2.4×10-5mol•L-1 | D. | 3.2×10-6mol•L-1 |
分析 先计算出溶液中氢氧根离子的物质的量浓度,然后根据Pb(OH)2的溶度积及c(Pb2+)=$\frac{Ksp}{{c}^{2}(O{H}^{-})}$进行计算.
解答 解:由Pb(OH)2的溶度积为1.2×10-15,pH=8,c(OH-)=10-6mol•L-1,则c(Pb2+)=$\frac{Ksp}{{c}^{2}(O{H}^{-})}$=$\frac{1.2×1{0}^{-15}}{(1{0}^{-6})^{2}}$mol/L=1.2×10-3mol•L-1,故选A.
点评 本题考查难溶电解质的溶解平衡,为高频考点,侧重考查学生应用电离平衡常数、溶度积来分析解决问题,注重了对数据的分析和应用,较好的训练学生分析解决问题的能力,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{17}^{37}$Cl表示质子数为17、中子数为20的核素 | |
| B. | 乙二醇(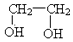 )和甘油( )和甘油(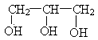 )互为同系物 )互为同系物 | |
| C. | 干冰和CO2互为同分异构体 | |
| D. | 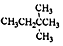 的名称是3,3-二甲基丁烷 的名称是3,3-二甲基丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 可能含有一个酯基和一个碳碳双键 | B. | 可能含有一个醛基和一个羰基 | ||
| C. | 可能含有一个环和一个酯基 | D. | 可能含有一个醛基和一个碳碳叁键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性:X<Z<W | |
| B. | Y的阳离子半径比W的阴离子半径小 | |
| C. | X、Z、W最高价氧化物对应水化物酸性的强弱顺序为X<Z<W | |
| D. | 室温下,含Y元素的盐形成的水溶液其pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H6 | C5H12 | C8H18 |
| A. | C13H28 | B. | C17H36 | C. | C26H54 | D. | C53H108 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某化学兴趣小组进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | NaCl溶液是电解质 | |
| B. | 电解质在电流的作用下才发生电离 | |
| C. | NaCl溶液中的水电离出大量的离子 | |
| D. | NaCl在水溶液中存在自由移动的离子是溶液能导电的原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Na+、SO42-、Ba2+ | ||
| C. | K+、MnO4-、NH4+、Cl- | D. | Ca2+、K+、HCO3-、NO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com