


科目:高中化学 来源: 题型:
下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①________,⑥________,⑦________
(2)画出原子的结构示意图:④__________,⑧__________
(3)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述 中能证明这一事实的是( )
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)第三周期(除稀有气体元素)中原子半径最大的元素是 (填序号),跟它同周 期原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程下:
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,该化合物是(填分子式) 分子的空间构型为:
查看答案和解析>>
科目:高中化学 来源:2010年内蒙古赤峰市田家炳中学高二上学期期中考试化学试卷 题型:实验题
下表是元素周期表的一部分,回答下列有关问题: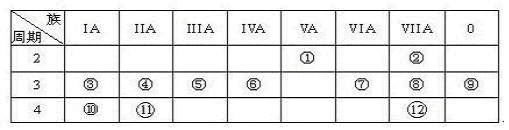
(1)写出下列元素符号:①________,⑥________,⑦________
(2)画出原子的结构示意图:④__________,⑧__________
(3)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是( )
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)第三周期(除稀有气体元素)中原子半径最大的元素是 (填序号),跟它同周 期原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程下:
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,该化合物是(填分子式) 分子的空间构型为:
查看答案和解析>>
科目:高中化学 来源:2014届山东省文登市高三上学期期中统考理综化学试卷(B)(解析版) 题型:填空题
要准确掌握化学用语及常用计量方法。按要求回答下列问题:
(1)NA表示阿伏加德罗常数。28g乙烯和环丁烷(C4H8)的混合气体中含有____NA个碳原子;分子总数为NA个的NO2和CO2混合气体含______ NA个氧原子数;1mol37Cl中,中子数比质子数多_______ NA个;1L 1mol/LFe2(SO4)3溶液中含_____NA个SO42-离子。
(2)图中A、B分别是某微粒的结构示意图,回答下列问题:

①若A表示某元素的原子,则y= 。
②若B表示某稀有气体元素的原子,则该元素的单质的化学式为 ,若B是阴离子的结构示意图,则x的取值范围是________________。
(3)RxO42-中R的化合价为___________(用含x 的式子表示),当0.3 mol RxO42-完全反应,生成RO2时,转移0.6 mol电子,则x=__________。
(4)将7.8 g镁铝合金与100mL 稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐46.2 g,则原硫酸的物质的量浓度为______________。
查看答案和解析>>
科目:高中化学 来源:2010年内蒙古赤峰市高二上学期期中考试化学试卷 题型:实验题
下表是元素周期表的一部分,回答下列有关问题:

(1)写出下列元素符号:①________,⑥________,⑦________
(2)画出原子的结构示意图:④__________,⑧__________
(3)元素⑦与元素⑧相比,非金属性较强的是 (用元素符号表示),下列表述 中能证明这一事实的是( )
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(4)第三周期(除稀有气体元素)中原子半径最大的元素是 (填序号),跟它同周 期原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程下:
(5)已知某元素原子最外层电子数是其次外层电子数的2倍,该元素可以与⑧形成一种AB4型的化合物,该化合物是(填分子式) 分子的空间构型为:
查看答案和解析>>
科目:高中化学 来源:同步题 题型:不定项选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com