
某工厂的废气中含有CO、SO2、NO等有毒气体,为了更有效地治理该废气,某研究小组分别设计了如下两个方案:
方案(1):治理含CO、SO2的烟道气,以Fe2O3作催化剂,将CO、SO2在380℃时转化为S和一种无毒气体。
已知:ⅰ.硫的熔点112.8℃,沸点444.6℃;
ⅱ.反应每得到1mol硫,放出270kJ的热量。
①写出该治理烟道气反应的热化学方程式: 。
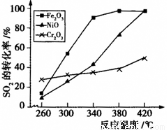
②其他条件相同,催化剂不同时,上述反应中SO2的转化率随反应温度的变化如下图。不考虑催化剂价格因素,生产中选Fe2O3作催化剂的主要原因是 。
方案(2):用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g) 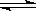 N2(g)+CO2(g)。向某容积为2L 的密闭容器中加入NO和足量的活性炭(固体试样体积忽略不计),恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g)。向某容积为2L 的密闭容器中加入NO和足量的活性炭(固体试样体积忽略不计),恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.32 | 0.32 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.34 | 0.34 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.17 | 0.17 |
①10min~20min以v(CO2)表示的反应速率为 。
②根据表中数据,T1℃时该反应的平衡常数为 (保留两位有效数字)。
③下列各项能作为判断该反应达到平衡状态标志的是 (填序号字母)。
A.容器内压强保持不变
B.2v正(NO)=v逆(N2)
C.容器内CO2的体积分数不变
D.混合气体的密度保持不变
④30min时改变某一条件,反应重新达到平衡,则改变的条件可能是 ;
⑤一定温度下,随着NO的起始浓度增大,NO的平衡转化率 (填“增大”、“减小”或“不变”)
⑥50min时,保持其他条件不变,往容器中再充入0.32 mol NO和0.34mol CO2,平衡将向 方向移动。
科目:高中化学 来源:2016-2017学年吉林省高一上期初化学卷(解析版) 题型:选择题
下列各组物质,按化合物、单质、混合物顺序排列的是
A.生石灰、白磷、冰水混合物 B.烧碱、液氧、碘酒
C.干冰、铁、氯化氢 D.纯碱、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上第一次考试化学卷(解析版) 题型:选择题
下列溶液中,与200mL 0.5mol/L MgCl2溶液所含的Cl-物质的量浓度相同的是
A.100mL 0.25mol/L CaCl2溶液 B.50ml 1mol/L KCl溶液
C.50ml 0.5mol/L NaCl溶液 D.200mL 0.25mol/L AlCl3溶液
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第一次月考化学试卷(解析版) 题型:填空题
分现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
X | 地壳中含量最高的非金属元素 |
Y | M层比K层多1个电子 |
Z | 最外层电子数为内层电子数的0.6倍 |
W | 与氯形成的氯化物是生活中常用的调味品 |
(1)X形成的双原子分子的结构式为 ,X形成的氢化物的沸点在同族元素形成的氢化物中是 (填“最高”或“最低”),原因是 。
(2)金属冶炼Y单质的化学方程式为 。
(3)Y单质与W元素的最高价氧化物对应水化物恰好反应完全,向反应后的溶液中通入过量的CO2,发生反应的离子方程式为 。
(4)单质Cu在一定条件下与足量Z元素形成的强酸浓溶液反应生成的气体是 (填化学式),检验该气体的常用试剂 。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法错误的是( )
A.弱电解质溶液中至少存在两种共价化合物分子
B.强电解质都是离子化合物,弱电解质都是共价化合物
C.NH3属于非电解质,但其水溶液能够导电
D.同位素单质混合在一起一般是纯净物
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上第12次周测化学卷(解析版) 题型:选择题
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是
A. 元素A、B组成的化合物常温下一定呈气态
B. 单质沸点:C>D>E
C. 工业上常用电解法制备元素C、D、E的单质
D. 离子半径:r(C)>r(D)>r(E)
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10月月考化学试卷(解析版) 题型:填空题
二甲醚(CH3OCH3)和甲醇(CH3OH)被称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:

请填空:
(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g) CO(g)+3H2(g) △H>0。将1.0molCH4和2.0molH2O通人反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)=________。该反应平衡常数的表达式:_____________。
CO(g)+3H2(g) △H>0。将1.0molCH4和2.0molH2O通人反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)=________。该反应平衡常数的表达式:_____________。
(2)已知:CH3OCH3 (g)+3O2(g)=2CO2(g)+3H2O(g) △H=-1323 KJ/mol;
2H2(g)+O2(g)=2H2O(g) △H=-484 KJ/mol;
CO的燃烧热:283KJ/mol。
在一定条件下,反应室2的可逆反应除生成二甲醚外还生成了气态水,该热化学方程式为_______________。(本题涉及的条件均在同一条件下)
(3) 绿色电源“二甲醚-氧气燃料电池”的工作原理如右图所示,写出X电极的电极反应式_______________

(4)反应室3中在催化剂作用下发生如下反应:CO(g) +2H2(g)  CH3OH(g)。对此反应进行如下研究:
CH3OH(g)。对此反应进行如下研究:
①在容积为1L的密闭容器中分别充入1molCO和2molH2,实验测得甲醇的物质的量和温度、时间的关系曲线如图1所示。
则:该正反应的△H___________0(填“<”、“>”或“=")。
②在容积均为1L的a、b、c三个相同密闭容器中分别充入1mol CO和2mol H2,三个容器的反应温度分别为T1、T2、T3,在其他条件相同情况下,实验测得反应均进行到5min时甲醇的体积分数如图2所示。下列说法正确的是_______________
A.a、b、c三容器5min时的正反应速率大小为:b>a>c
B.达到平衡时,a、b、c三容器中CO转化率为a>b>c
C.5min时,a、b、c三容器中的反应均可能达到平衡状态。
D.将容器b中的平衡状态转变到容器c中的平衡状态,可采取的措施有升温或减压
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上10月月考化学试卷(解析版) 题型:选择题
对下列物质的化学用语书写正确的是( )
A.乙烯的结构简式为CH2CH2
B.羟基的电子式: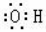
C.Ca2+的结构示意图为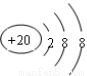
D.乙醇的分子式:CH3CH2OH
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期第一次月考化学卷(解析版) 题型:选择题
(金属镍有广泛的用途。粗镍中含有少量杂质Fe、Zn、Cu、Pt, 可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是( )
可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是( )
A.阳极发生还原反应,其电极反应式:Ni2++2e-=Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com