
(1)____________________________________________。
(2)____________________________________________。
科目:高中化学 来源: 题型:阅读理解

| 实验步骤 | 现象和结论 |
| 步骤一:取C中的少量固体样品于试管中,滴加足量蒸馏水至完全溶解,然后将溶液分别置于a、b试管中. | |
| 步骤二:向a试管中滴加BaCl2溶液,静置. | 无明显现象,证明固体中不含Na2CO3 |
| 步骤三: 取a试管的上层清液于c试管中 取a试管的上层清液于c试管中 加入适量氢氧化钡溶液 加入适量氢氧化钡溶液 |
产生白色沉淀 产生白色沉淀 证明固体中含有碳酸氢钠 证明固体中含有碳酸氢钠 |
| 步骤四: 向试管b中加入过量稀硝酸溶液 向试管b中加入过量稀硝酸溶液 再滴加少量硝酸银溶液 再滴加少量硝酸银溶液 |
有白色沉淀生成 有白色沉淀生成 则证明固体中含有NaCl. |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验操作 |
| I | 取一定质量的FeCO3固体置于坩埚中,高温燃烧至质量不再减轻,冷却至室温. |
| II | 取少量实验步骤I所得固体放于一洁净的试管中,用足量的稀硫酸溶解. |
| III | 向实验步骤II所得溶液中滴加KSCN溶液,溶液变红. |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
我国有着丰富的海水资源,海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子。镁因其合金性能卓越,在汽车、飞机制造方面很重要,有“国防金属”之称。发达国家多数从海洋中提镁,中国海水提镁技术也在不断进步。海水中虽含镁离子很多,但它是很分散的(1.28 g?L-1),要提取镁首先应让镁离子与其它离子等分离。
请回答下列问题:
(1)某化学兴趣小组利用煅烧海边贝壳所得产物,投入浓缩的海水中,最终变成了Mg(OH)2浊液。请写出最后一步反应的离子方程式: 。
(2)已知,氧化镁熔点2852℃,氯化镁的熔点714℃。无水氯化镁是工业制取镁的原料。试写出实验室蒸发氯化镁溶液制取无水氯化镁必需的实验仪器是 ;某同学对蒸发得到的固体,用酒精喷灯加热却不能熔化,请你试分析原因

(3)火力发电在江苏的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题。利用海水脱硫是一种有效的方法,其工艺流程如下图所示:
①天然海水的pH≈8,试用离子方程式解释天然海水呈弱碱性的原因 。
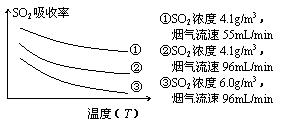 ②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如右图所示。请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议: 。
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如右图所示。请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议: 。
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,使用氧气将其氧化的化学原理是 (任写一个化学方程式或离子方程式)。氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com