
【题目】一种碳纳米管新型二次电池的装置如图所示。下列说法中正确的是
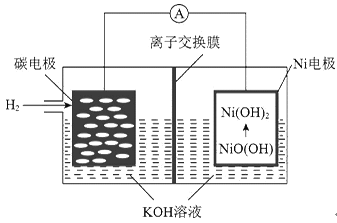
A. 离子交换膜选用阳离子交换膜(只允许阳离子通过) B. 正极的电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
C. 导线中通过1mol电子时,理论上负极区溶液质量增加1g D. 充电时,碳电极与电源的正极相连
科目:高中化学 来源: 题型:
【题目】下列关于金属的说法中,不正确的是( )
A. 各种金属都能与盐酸发生置换反应 B. 金属具有良好的延展性
C. 金属都能导电 D. 根据金属与酸反应置换出氢的难易程度可比较金属的活泼性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把9.0g乙二酸和某二元醇混合,在一定条件下完全酯化,生成W g环酯和3.6g水,则该醇的相对分子质量可以表示为( )
A. 10W﹣54 B. 5W+13.5 C. 45(W﹣3.6) D. 2W+10.8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3
C. 加入催化剂有利于氨的合成
D. 工业制取金属钾Na(l)+KCl(l)![]() NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K变成蒸气从反应混合物中分离出来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 铵盐不稳定,受热分解都产生氨气
B. N2是空气中的主要成分之一,雷雨时可直接转化为NO2
C. 由于浓硫酸有强氧化性,因此不能用铁罐贮存浓硫酸
D. 浓硝酸不稳定,实验室保存在棕色试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,往某浓度的氯水中滴人Na2S03溶液的pH变化如图所示,下列离子浓度的关系错误的是

A. a点:c(H+)>c(Cl-)>c(ClO-)
B. b点:l/2 c(Cl-)=c(SO42-)=0.005mol·L-1
C. 点:c(Na+)=2c(HSO3-)+2c(SO32-)
D. d 点:c(Na+)=c(Cl-)+c(HSO3-)+2c(SO32-)+2c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、硫和氮的氧化物与大气污染密切相关,对CO2、SO2和NO2的研究很有意义.
(1)科学家发现NOx与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
I:2NO2(g)+NaCl(g) ![]() NaNO3(g)+ClNO(g) ΔH1<0(平衡常数为K1)
NaNO3(g)+ClNO(g) ΔH1<0(平衡常数为K1)
II:2NO(g)+ Cl(g) ![]() 2ClNO(g) ΔH2<0(平衡常数为K2)
2ClNO(g) ΔH2<0(平衡常数为K2)
III:4NO2(g)+2NaCl(g) ![]() 2NaNO2(g)+2NO(g)+Cl2(g) ΔH3 (平衡常数为K3)
2NaNO2(g)+2NO(g)+Cl2(g) ΔH3 (平衡常数为K3)
反应III中K3=___________(用K1、K2表示),ΔH3 =_______(用ΔH1、ΔH2表示)。若反应II在恒温、恒容条件下进行,能判断该反应一定达到平衡状态的标志是________________。
A.容器内混合气体的压强保持不变
B.v正(NO)=v逆(Cl2)
C.容器内混合气体的密度保持不变
D.容器内混合气体的平均相对分子质量保持不变
(2)汽车尾气中排放的NOx和CO会污染环境,在汽车尾气系统中安装催化转化器,可有效降低NOx和CO的排放,为了模拟应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO(g)和CO(g)的浓度如下表:
N2(g)+2CO2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO(g)和CO(g)的浓度如下表:
时间/S | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(10-4mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(10-3mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
平衡时,NO的转化率ɑ(NO)=_________________,
此溫度下,该反应的平衡常数K=_______________。
(3)科学家提出由CO2制取C的工艺如图所示。已知:在重整系统中n(FeO): n(CO2)=5 : 1则在“热分解系统”中,FexOy的化学式为__________________。

(4)NQx可“变废为宝”,由NO电解可制备NH4NO3,其工作原理如图所示(M、N为多孔电极)。为使电解产物全部转化为NH4NO3,需向电解产物中补充适量NH3。电解时M和电源________极(填“正或负”)相连,书写N极发生的电极反应式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从薄荷中提取的薄荷醇可制成医药。薄荷醇的结构简式如下图,下列说法正确的是
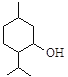
A. 薄荷醇分子式为C10H20O,它是环己醇的同系物
B. 薄荷醇的分子中至少有12个原子处于同一平面上
C. 薄荷醇在Cu或Ag做催化剂、加热条件下能被O2氧化为醛
D. 在一定条件下,薄荷醇能发生取代反应、消去反应和聚合反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com