
 .
. 或
或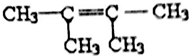 .
.分析 (1)烃含有C、H两种元素,某烃A0.2mol在氧气的充分燃烧后生成化合物B、C各1.2mol,即生成CO2、H2O各1.2mol,则1mol烃中含有6molC,12molH原子,A分子式为C6H12;
(2)根据燃烧方程式计算A的物质的量、消耗氧气的物质的量,再根据m=nM计算烃A的质量,根据V=nVm计算消耗氧气的体积;
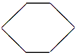
(3)若烃A不能使溴水褪色,说明有机物中不含C=C官能团,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,应为环己烷;
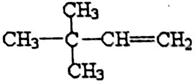
(4)若烃A能使溴水褪色,在催化剂作用下与H2加成,其加成产物经测定,分子中含有4个甲基,生成物为 、
、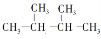 ,说明分子中含有1个C=C键,相邻两个碳原子都含有H原子为C=C双键位置,据此确定A的结构简式;
,说明分子中含有1个C=C键,相邻两个碳原子都含有H原子为C=C双键位置,据此确定A的结构简式;
(5)若烃A能使溴水褪色,且分子中所有碳原子共平面,则C=C双键中不饱和C原子连接四个甲基,据此确定A的结构简式.
解答 解:(1)烃含有C、H两种元素,某烃A0.2mol在氧气的充分燃烧后生成化合物B,C各1.2mol,即生成CO2、H2O各1.2mol,则1mol烃中含有6molC,12molH原子,分子式为C6H12,
故答案为:C6H12;
(2)C6H12完全燃烧,生成3molCO2和H2O,则:
C6H12+9O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+6H2O,
1mol 9mol 6mol 6mol
0.5mol 4.5mol 3mol 3mol
当生成3molCO2和H2O时,需要0.5molC6H12,m(C6H12)=0.5mol×84g/mol=42g,
需要氧气的体积为V(O2)=4.5mol×22.4L/mol=100.8L,
故答案为:42;100.8;
(3)若烃A不能使溴水褪色,说明有机物中不含C=C官能团,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,应为环己烷,结构简式为 ,故答案为:
,故答案为: ;
;
(4)若烃A能使溴水褪色,在催化剂作用下与H2加成,其加成产物经测定,分子中含有4个甲基,生成物为 、
、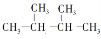 ,说明分子中含有1个C=C键,相邻两个碳原子都含有H原子为C=C双键位置,故A的结构简式为:
,说明分子中含有1个C=C键,相邻两个碳原子都含有H原子为C=C双键位置,故A的结构简式为: 或
或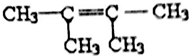 ,
,
故答案为: 或
或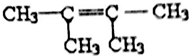 ;
;
(5)比烃A少2个碳原子的烯烃同系物有:CH3CH2CH=CH2、CH3CH=CHCH3、(CH3)2C=CH2,其中能和H2发生加成反应生成2-甲基丙烷的烯烃为(CH3)2CC=CH2,名称是:2-甲基丙烯,
故答案为:3;2-甲基丙烯.
点评 本题考查有机物推断与限制条件同分异构体的书写,题目难度中等,注意掌握烯烃的结构与性质.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:选择题
| A. | 含有共价键的化合物一定为共价化合物 | |
| B. | 含有离子键的化合物一定为离子化合物 | |
| C. | 吸热反应中,旧化学键断裂吸收能量;放热反应中,旧化学键断裂放出能量 | |
| D. | 吸热反应中,新化学键形成吸收能量;放热反应中,新化学键形成放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁 | B. | N2 | C. | 铜 | D. | 硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
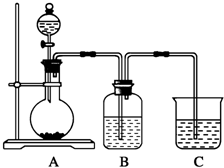 某同学设计实验以探究元素性质的递变规律,实验装置如图所示.
某同学设计实验以探究元素性质的递变规律,实验装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从ⅢB族到ⅡB族之间的10个纵行的元素都是金属元素 | |
| C. | 非极性键也可能存在于离子化合物中 | |
| D. | 双原子分子中的共价键,可能是极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,0.4g D2气体分子含有的中子数小于0.2NA | |
| B. | 含有0.32g氧元素的二氧化硅中含有的硅氧键数目为0.02NA | |
| C. | 11.2L Cl2通入足量氢氧化钠溶液中充分反应,转移的电子数等于0.5NA | |
| D. | 7.8g过氧化钠粉末与足量二氧化硫反应转移的电子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com