
【题目】下列说法不正确的是
A. 溴在海水中以化合态形式存在
B. 从海水中提取溴要经历浓缩、氧化和提取三个步骤
C. 提取金属镁是电解氯化镁的熔融液
D. 溴在常温下是液态,其颜色与氯气颜色相同
科目:高中化学 来源: 题型:
【题目】在NaClO和NaCl混合溶液中能大量共存的离子组是( )
A.H+、Al3+、NH4+、SO42﹣
B.Ag+、NO3﹣、Na+、Ba2+
C.Fe2+、NO3﹣、SO42﹣、Na+
D.K+、CO32﹣、SO42﹣、OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.常温常压下,23g NO2含有NA个氧原子
B.标准状况下,22.4L H2O含有NA个H2O分子
C.含10 NA个电子的N2分子的物质的量是1mol
D.0.1mol/L的Ba(OH)2溶液中,OH﹣的个数为0.2NA个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】惰性电极电解NaCl溶液或CuSO4溶液都得到三种产物A、B、C,各物质之间的转化关系如下图所示(图中参与反应和生成的水都已略去)。已知甲是短周期元素的单质,它是日常生活中常用的包装材料。

回答下列问题:
(1)若电解的是NaCl溶液:
①甲与A反应的化学方程式是________________________________。
②E与少量CO2反应的离子方程式是________________________________。
③常温下,若电解100mL 0.1 mol/L NaCl溶液,阴、阳两极各产生112mL气体(标准状况),则所得溶液的pH为___(忽略反应前后溶液的体积变化及气体溶于水的影响)。
(2)若电解的是CuSO4溶液,加热时,A的浓溶液可与B发生反应:
①A的浓溶液与B反应过程中,A的浓度随时间变化的图像正确是_________。

②E的化学式是______________;电解时阳极的电极反应式是___________________。
③若CuSO4溶液足量,电解后要恢复原来的浓度可加入 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为实验室从海带中提取碘单质的流程示意图,判断下列说法错误的是( ) 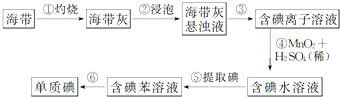
A.步骤①需要用到蒸发皿
B.步骤③需要过滤装置
C.步骤⑤需要用到分液漏斗
D.步骤⑥需要蒸馏装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“探险队员”﹣﹣盐酸,不小心走进了化学迷宫,迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过. 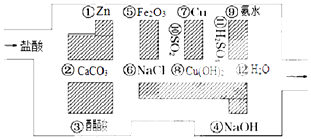
(1)请你帮助它走出迷宫(用图中物质前的序号连接起来表示所走的路线) .
(2)在能“吃掉”盐酸的化学反应中,写出属于酸和碱中和反应的方程式:
(3)在不能与盐酸反应的物质中,属于非电解质的是(填写物质序号).
(4)写出物质②的电离方程式
(5)写出盐酸与碳酸钙反应的离子方程式:
(6)写出Ag++Cl﹣=AgCl↓对应的化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用98%的浓硫酸(ρ=1.84gcm﹣3)配制成浓度为0.5molL﹣1的稀硫酸500mL.
(1)所需仪器除烧杯,量筒,玻璃棒外,还需要实验仪器才能完成该实验.
(2)简要回答下列问题:①所需浓硫酸的体积为mL.②量筒量取浓硫酸后发现量筒内壁还附有硫酸,用水洗净量筒后将洗液一起转移至容量瓶,将使溶液浓度; (填“偏高”、“偏低”、“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中二氧化硫、氮氧化物和可吸入颗粒物是雾霾主要组成.某课题组用汽车尾气为原料探究二氧化硫、氮氧化物的化学性质.
(1)I.汽车尾气(含有烃类、CO、SO2与NO等物质),冶理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂).它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化.写出一氧化碳与一氧化氮反应的化学方程式: Ⅱ.课题组欲在绿色环保的条件下探究大气污染物SO2的性质,设计如图实验装置.请回答:
B、C、D分别用于检验SO2的漂白性、还原性和氧化性,则B中所盛试剂为;C中反应的离子方程式为 .
(2)为了实现绿色环保的目标,制取SO2装置最好选择 . (A1或A2装置)用氨水吸收尾气中的SO2 , “吸收液”中可能含有OH﹣、SO32﹣、SO42﹣、HSO3﹣等阴离子.请回答:
(3)氨水吸收过量SO2的反应的离子方程式为
(4)已知亚硫酸氢盐一般易溶于水,SO2也易溶于水.现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/LHNO3、1mol/LBaCl2溶液、l mol/LBa(OH)2溶液、品红溶液、蒸馏水.请设计实验证明“吸收液”中存在SO32﹣、HSO3﹣ , 完成下表的实验操作、预期现象和结论:
实验操作 | 预期现象与结论 |
步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取l mol/L BaCl2溶液向小烧杯滴加直至过量. | 若出现白色浑浊,则溶液中存在SO32﹣或 SO42﹣ . |
步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体 . |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com