
反应A(g)+B(g)→C(g) ΔH分两步进行:①A(g)+B(g)→X(g)ΔH1 ②X(g)→C(g) ΔH2,反应过程中能量变化如图所示,E1表示A(g)+B(g)→X(g)的活化能,下列说法正确的是( )
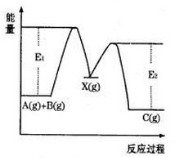
A.ΔH1=ΔH-ΔH2>0
B.X是反应A(g)+B(g)→C(g)的催化剂
C.E2是反应②的活化能
D.ΔH=E1-E2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014年高考化学指导冲关 第9练非金属及其化合物练习卷(解析版) 题型:选择题
下列解释实验事实的反应方程式不正确的是( )
A.盛放烧碱的试剂瓶不能用玻璃塞:SiO2+2NaOH=Na2SiO3+H2O
B.用烧碱溶液吸收氯气:Cl2+2OH-=Cl-+ClO-+H2O
C.用KSCN溶液检验Fe3+:Fe3++3SCN-=Fe(SCN)3
D.酸性KI淀粉溶液久置后变蓝:4I-+O2+2H2O=2I2+4OH-
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第4练物质结构与元素周期律练习卷(解析版) 题型:选择题
短周期元素A、B、C、D的原子序数依次增大,它们的核电荷数之和为32,原子最外层电子数之和为10;A与C同主族,B与D同主族,A、C原子最外层电子数之和等于B原子次外层电子数,则下列叙述正确的是( )
A.D元素处于元素周期表第3周期ⅥA族
B.四种元素原子半径大小顺序是A<B<C<D
C.B、D的最高价氧化物具有相似的物理性质和化学性质
D.一定条件下,B单质能置换出D单质,C单质能置换出A单质
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第3练化学反应与能量变化练习卷(解析版) 题型:填空题
某种优质燃油由甲、乙两种有机物混合而成,甲、乙两种物质含有C、H、O三种元素中的两种或三种。已知甲、乙及CO、H2的燃烧热如下:
物质 | 甲 | 乙 | CO | H2 |
燃烧热/(kJ·mol-1) | 1 366 | 5 518 | 283 | 286 |
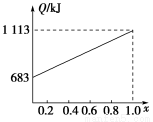
取甲、乙按不同比例混合的燃油23 g,在足量的O2中燃烧时,放出的热量Q与混合物中乙的物质的量分数x的关系如图所示。试求:
(1)乙的相对分子质量Mr(乙)=________。
(2)160 g由甲、乙以等物质的量混合而成的燃油在347.2 L O2中恰好完全燃烧,得492.8 L气体,冷却到室温时,还剩余224 L(气体体积均在标准状况下测定)。由此可求得混合物中,C、H、O的原子个数比为________。甲、乙的分子式为:甲________;乙________。
(3)1 mol由甲、乙以等物质的量混合而成的燃油在一定量的O2中燃烧,放出热量2 876 kJ,则反应中生成CO________mol。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第3练化学反应与能量变化练习卷(解析版) 题型:选择题
已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)
ΔH=-57.3 kJ/mol下列结论正确的是( )
A.碳的燃烧热的数值大于110.5 kJ/mol
B.①的反应热ΔH为221 kJ/mol
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第2练氧化还原反应和离子反应练习卷(解析版) 题型:选择题
Na2FeO4是一种高效多功能水处理剂,一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2 +O2↑。下列对此反应的说法中,不正确的是( )
+O2↑。下列对此反应的说法中,不正确的是( )
A.方框中的物质为Na2SO4
B.Na2O2既是氧化剂,又是还原剂
C.Na2FeO4既是氧化产物,又是还原产物
D.2 mol FeSO4发生反应时,反应中共转移8 mol电子
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第1练物质分类化学用语和常用计量练习卷(解析版) 题型:选择题
现取m g镁铝合金在一定浓度的稀硝酸中恰好完全溶解(硝酸的还原产物只有NO),向反应后的混合溶液中滴加b mol/L NaOH溶液,当滴加到V mL时,得到沉淀质量恰好为最大值n g,则下列有关该实验的说法中正确的是( )
①沉淀中OH-的质量为(n-m)g
②恰好溶解后溶液中的NO3—的物质的量为  mol
mol
③反应过程中转移的电子数为 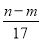 mol
mol
④标准状况下生成NO的体积为  L
L
⑤与合金反应的硝酸的物质的量为( +
+ )mol
)mol
A.5项 B.4项 C.3项 D.2项
查看答案和解析>>
科目:高中化学 来源:2014年高考化学指导冲关 第12练物质制备方案的设计与评价练习卷(解析版) 题型:实验题
亚硫酸盐是一种常见食品添加剂。为检测某食品中亚硫酸盐含量(通常以1 kg样品中含SO2的质量计)。某研究小组设计了如下两种实验流程:
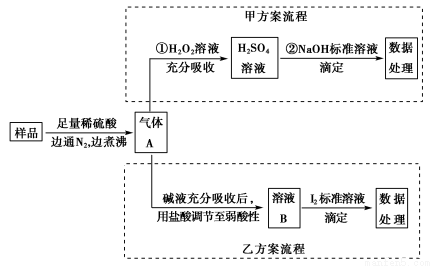
(1)气体A的主要成分是________。为防止煮沸时发生暴沸,必须先向烧瓶中加入________;通入N2的目的是________。
(2)写出甲方案第①步反应的离子方程式:________________________。
(3)甲方案第②步滴定前,滴定管需用NaOH标准溶液润洗,其操作方法是__________________________________________________________。
(4)若用盐酸代替稀硫酸处理样品,则按乙方案实验测定的结果________(填“偏高”“偏低”或“无影响”)。
(5)若取样品w g,按乙方案测得消耗0.010 00 mol·L-1I2溶液V mL,则1 kg样品中含SO2的质量是________g(用含w、V的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com