
科目:高中化学 来源:2016-2017学年内蒙古高二下月考二化学卷(解析版) 题型:选择题
在核磁共振氢谱中出现两组峰,其氢原子数之比为3:1的化合物是 ( )
A. B.
B.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二12月月考化学卷(解析版) 题型:选择题
除去下列物质中的杂质(括号内的物质),所使用的试剂 和主要操作都正确的是
和主要操作都正确的是
选项 | 物质 | 使用的试剂 | 主要操作 |
A | 乙醇(水) | 金属钠 | 蒸馏 |
B | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
C | 苯(苯酚) | 浓溴水 | 过滤 |
D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏林芝一中高一上期末化学试卷(解析版) 题型:选择题
物质能够表现出多种性质,也对应着多种分类方法。下列说法正确的是( )
A.由同种元素组成的物质一定是纯净物
B.CO是非金属氧化物,也是是酸性氧化物
C.稀豆浆是常见的胶体,故能发生丁达尔效应
D.有单质参加的化学反应一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏林芝一中高二上期末化学试卷(解析版) 题型:填空题
电解装置如图所示:
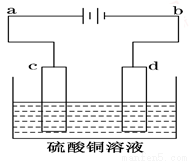
Ⅰ.当用惰性电极电解时,c为____________极,电极反应________d为____________极,电极反应______________,电解总反应的化学方程____________________
Ⅱ.(1)若用此装置进行铁上镀铜则c为__________(填铁或铜)d为___________(填铁或铜)电解液浓度_____________(增大,减小或不变)
(2)电 镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子___________mol.
镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子___________mol.
Ⅲ.若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极________(填图中的字母);若粗铜中还含有Au、Ag、Fe,则Fe以_______(填离子符号)形式进入溶液,c电极发生的反应______________,________________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一12月月考化学卷(解析版) 题型:实验题
聚合硫酸铁(简称PFS,化学式为[Fe(OH)n(SO4)3-n/2]m )是一种新型高效的无机高分子絮凝剂,广泛用于水的处理,现用一定质量的铁的氧化物(如下图)为原料来制取聚合硫酸铁。实验步骤如下: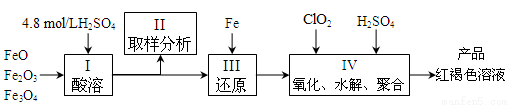
(1)实验室用18.4mol/L的浓硫酸配制250mL4.8mol/L的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需的玻璃仪器__________。定容操作中若俯视容量瓶刻度线,所配硫酸溶液浓度将___________(填“偏高”、“偏低”或“无影响”)
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是_______。
A.确定下一步还原所需铁的量 B.控制溶液中Fe2+与Fe3+含量比
C.确定氧化Fe2+所需ClO2的量 D.确保铁的氧化物酸溶完全
(3)写出步骤Ⅳ中用ClO2氧化Fe2+时的离子方程式:____________________。(还原产物为Cl-)
(4)为了分析产品聚合硫酸铁溶液中SO42-与Fe3+物质的量之比,有人设计了以下操作:
(I)取25mL聚合硫酸铁溶液,加入足量的BaCl2溶液,产生白色沉淀,白色沉淀经过过滤,洗涤、干燥后,称重,其质量为mg。
(II)另取25mL聚合硫酸铁溶液,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250mL溶液,取该溶液25.00mL与0.1000 mol/L V mL KMnO4酸性溶液恰好完全反应,MnO4-被还原为Mn2+。
回答下列问题:
① 根据(II)步骤中判断Cu2+、Fe2+、MnO4-、Fe3+氧化性由强到弱的顺序:__________。
② 聚合硫酸铁中SO42-与Fe3+的物质的量之比为____________(用含m、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一12月月考化学卷(解析版) 题型:选择题
己知下述三个实验均能发生化学反应①将铁钉放入硫酸铜溶液中 ②向硫酸亚铁溶液中滴入几滴氯水 ③将铜丝放入氯化铁溶液中下列判断正确的是
A.实验①中铁钉做氧化剂 B.实验②中Fe2+其有还原性
C.实验③中发生的是置换反应 D.上述实验证明氧化性:Fe3+> Fe2+>Cu2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高一上期中化学卷(解析版) 题型:填空题
焦亚硫酸钠(Na2S2O5)是常用食品抗氧化剂,常用于葡萄酒、果脯等食品中。
(1)Na2S2O5中硫元素的化合价是________,焦亚硫酸钠在空气中久置会与氧气反应生成连二硫酸钠 (Na2S2O6), 写出该反应的化学方程式,并标出该反应电子的转移方向和数目_________________;
(2)葡萄酒中的 Na2S2O5的使用量是以游离的 SO2 来计算的,SO2 的摩尔质量________。我国规定每升葡萄酒中SO2的最高含量是 0.25g,则一瓶 800mL 的葡萄酒中 SO2的物质的量不能超过___________(精确到 0.001 );
(3)世界卫生组织规定按照体重计算,每人每天摄入SO2的最大量应控制在 0.7mg/kg,如果一个人体重是60kg,那么他每天喝上述葡萄酒的量不超过 __________mL 就不会造成健康上的问题。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考三化学卷(解析版) 题型:选择题
在含有Cu(NO3)2、Mg(NO3)2、AgNO3的溶液中加入适量锌粉,首先置换出的是( )
A.Mg B.Cu C.Ag D.H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com