
��10�֣��������ϵã�HNO2��һ�������Ҳ��ȶ����ֽ�����NO��NO2�����ܱ�������ǿ��������������������Һ����Ҳ��һ�������������ܰ�Fe2��������Fe3����AgNO2��һ��������ˮ����������Ļ����
�Իش��������⣺
��1���������������������NaNO2��NaCl����________(�����)��
A���ⶨ��������Һ��pH B���ֱ���������Һ�еμӼ���
C�������������¼���KI��������Һ������ D�� ��AgNO3��HNO3�����Լ�������
��2������������Ѫ�쵰����Fe2��������ʳ��������(��NaNO2)������Ѫ�쵰���е�
Fe2��ת��ΪFe3�����ж�������ά����C�ɽⶾ��������������ȷ����________(�����)��
A���������α���ԭ B��ά����C�ǻ�ԭ��
C��ά����C��Fe3����ԭΪFe2�� D�����������ǻ�ԭ��
��3�� Fe�����ϡ���ᷴӦ������ȡFeSO4�����÷�Ӧ���õ�������Һ����Fe2��ת��ΪFe3����Ҫ����﴿������ѡ�õ�����Լ���________(�����)��
A��Cl2 B��Fe C��H2O2 D��HNO3
��4��ijͬѧ�����Ը��������Һ����NaNO2��Һ�У��۲쵽��ɫ��ȥ��ͬʱ����NO3-��Mn2+����д����Ӧ�����ӷ���ʽ��_____________________________________________��
��5����֪FeSO4��һ�������¿�ת��Ϊ�������(K2FeO4)�����������һ�����͡���Ч����ɫˮ����������ˮ�з�����Ӧ���������������塣���������Ϊˮ���������ӵ�������_______________________________________��
��10�֣�����1�� B��2�֣�
��2�� D��2�֣�
��3�� c��2�֣�
��4�� 6H����5NO2����2MnO4- ===NO3����2Mn2+��3H2O ��2�֣�
��5�� ��ˮ��������2�֣�
��������
�����������1��A�������������ᣬ�����������Ƶ���Һ�Լ��ԣ����Ȼ�����Һ�����ԣ��������֣�����B�����Ի���Ե���Һ�еμӼ��ȣ���Һ���ʻ�ɫ���������֣���ȷ��C�������������¼���KI��������Һ��������������������������������������������Ϊ�ⵥ�ʣ����۱���ɫ�����������𣬴���D����AgNO3��HNO3��Ӧ���ɳ������������ƣ��������֣�����ѡB��
��2��A���������ƽ�������������Ϊ�����ӣ���������ԭ����ȷ��B��ά����C�ɽ������ӻ�ԭΪ�������ӣ�����ά����C����ԭ������ȷ��C��ά����C�ɽ������ӻ�ԭΪ�������ӣ��ﵽ�ⶾ��Ŀ�ģ���ȷ��D������������������������ѡD��
��3����Fe2��ת��ΪFe3����Ҫ����﴿������ѡ�õ�����Լ��ǹ������⣬��Ϊ����������������ʱ������ԭΪˮ���������µ����ʣ���ѡC;
��4�������Ը��������Һ����NaNO2��Һ�У��۲쵽��ɫ��ȥ��ͬʱ����NO3-��Mn2+��˵��������������������ط���������ԭ��Ӧ��������������Ӻ������Ӻ�ˮ�����ӷ���ʽΪ6H����5NO2����2MnO4- ===NO3����2Mn2+��3H2O��
��5��������ؾ���ǿ�����ԣ����Կ�������ˮ������ͬʱ��ԭ���������ӻ��������������������壬�����������ã����Ի��ܶ�ˮ�������á�
���㣺�����������εļ������ʣ����ӷ���ʽ����д


 ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ���������ֵ������˵����ȷ����
A�������£�23g NO2����NA����ԭ��
B��1 L 0.1 mol?L-1�İ�ˮ����0.1NA��OH�D
C����״���£�22.4 L CCl4����NA ��CCl4����
D��1 mol Fe2+��������H2O2��Һ��Ӧ��ת��2NA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�ϲ�����У�����ϵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
���и���������ָ������Һ���ܴ����������
����ɫ��Һ�У�K+��Cu2+��Na+��SO42��
��pH��11����Һ�У�CO32����Na+��AlO2����NO3��
�ۼ���Al�ܷų�H2����Һ�У�Cl����HCO3����NO3����NH4+
������ˮ�������c��OH������10��13 mol��L��1����Һ�У�Na+��Ba2+��Cl����I��
����ʹ��ɫʯ����ֽ��Ϊ��ɫ����Һ��Na+��Cl����S2����ClO��
��������Һ�У�Fe2+��Al3+��NO3����Cl��
A���٢ڢ� B���ڢ� C���ڢܢ� D���ۢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ�ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ����ȷ����
A��0.5mol/L��NaHSO3��Һ��1.0mol/L��NaClO��Һ�������ϣ�
HSO3����ClO����SO42����Cl����H��
B���������������������2Fe(OH)3��6H��+2I-��2Fe2++I2��6H2O
C��Ư����Һ�м��Ȼ�����Һ�����������ɫ������
Fe3����3ClO����3H2O��Fe��OH��3����3HClO
D��NH4HSO4��ϡ��Һ����μ���Ba(OH)2��Һ��SO42��ǡ�ó�����ȫ��NH4++H++SO42-+Ba2++2OH-=NH3?H2O+BaSO4��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ�ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��Ӧ����2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O��
��K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+Cr2(SO4)3+K2SO4+7H2O��
��Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4�����н�����ȷ����
A���٢ڢ۾���������ԭ��Ӧ
B��������ǿ��˳���ǣ�K2Cr2O7��Fe2(SO4)3��I2
C����Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ6��1
D����Ӧ����0.1mol��ԭ����ʧȥ������Ϊ1.2��1022
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���û�ѧʵ����Լ��������е�һЩ���ʡ��±��и������ʵļ����ܽ�������������ʶ����ֳ�������ѧ�Դ������
| ����������� | ���� |
A | ��ҵ�ƾ����״ס�ʳ��ˮ | �ÿڳ� |
B | N2 ��O2���� CO2������ | ��ȼ�ŵ�ľ�����飬�۲�ľ��ȼ����� |
C | ����ά��˿���� | ���գ���ȼ�ղ�������ζ���۲�ȼ������ͻҽ� |
D | ���ʣ��Ȼ��ء�����ء����[Ca3(PO4)2] | ����ۣ��ټ�ˮ���۲��Ƿ�����ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ܴﵽʵ��Ŀ�ĵ���
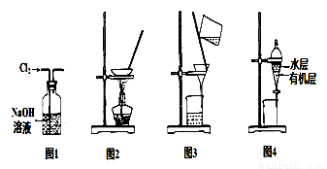
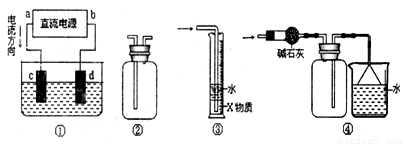

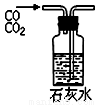
A����ȥFe��OH��3�����е�FeCl3 B������ռ������������ն���İ���
C�������Ҵ������� D����ȥ��������CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭����У������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
���л��к��ߵķ�Ӧ���ڷ�Ӧ�в�����ȫ���ĵ��ǣ� ��
A������������CO2��COͨ������Na2O2���Թ��в������õ����ȼ
B��������ʵ����ĸɱ���CaO�Ļ�����мӼ���ˮ
C����1molCu���ں�2molH2SO4��Ũ��Һ�м���
D����ǿ����������£��������Ca(ClO)2��Һ��ͨ��������CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������Э����߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������һ����Դ��������Ҫ�ɷ���CH4��0��5molCH4��ȫȼ������CO2��Һ̬ˮʱ�ų�445kJ���������������Ȼ�ѧ����ʽ����ȷ����
A��2CH4(g) + 4O2(g) = 2CO2(g) + 4H2O(l) ��H����890kJ��mol��1
B��CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ��H����890kJ��mol��1
C��CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) ��H����890kJ��mol��1
D��1/2CH4(g) + O2(g) = 1/2CO2(g) + H2O(l) ��H����890kJ��mol��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com