
常见元素X、Y、Z、W的原子序数依次增大,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
X的基态原子核外只有三个能级,且各能级电子数相等 |
|
Y |
Y的基态原子最外层电子数是其内层电子总数的2.5倍 |
|
Z |
Z的基态价电子结构为nsn-1 |
|
W |
W单质常在火山口附近被发现,其氧化物是造成酸雨的主要原因之一 |
(1)Y位于元素周期表第 周期 族,其基态原子未成对电子有 个。
(2)X的电负性比W的 (填“大”或“小”);Y的最简单气态氢化物比X的最简单气态氢化物易液化,其主要原因是 。
(3)Z与同周期左右相邻的两种元素的原子相比较,三者第一电离能由大到小的顺序为 (用元素符号表示)。Y和Z形成的化合物为 晶体,该物质遇水强烈水解的化学方程式为 。
(4)在一定温度下,向一个容积不变的密闭容器中充入1molY2和3mol氢气,发生反应:Y2(g)+3H2(g) 2YH3(g) ΔH=-akJ/mol。在该条件下达到平衡时放出的热量为bkJ,其平衡常数表达式K= 。若起始向此容器中充入2molYH3,在相同温度下达到平衡时,反应过程中吸收的热量为ckJ,则a、b、c三者之间的关系为 (用一个式子表示)。
(1)2,VA,3 (各1分,共3分)
(2)小,氨分子之间可以形成氢键 (各1分,2分)
(3)Mg>Al>Na,离子,Mg3N2+6H2O=3Mg(OH)2+2NH3↑ (各2分,6分)
(4)c2(NH3)/[c(N2)c3(H2)] a=b+c (各2分,4分)
【解析】
试题分析:根据题意知X、Y、Z、W分别是C、N、Mg、S;
N位于元素周期表的第二周期第VA族,其基态原子核外电子排布式为1S22S2P3,共有3个未成对电子;
C的电负性比S的要小,NH3比CH4易液化是因为氨分子间存在氢键;
根据元素周期率知同一周期元素从左到右第一电离能逐渐增大,但镁的最外层是3S2,属全充满结构,较稳定,第一电离能较后面的铝要大,Mg3N2是离子晶体,与水反应的方程式是Mg3N2+6H2O=3Mg(OH)2+2NH3↑;
工业合成氨的平衡常数表达式是K= c2(NH3)/[c(N2)c3(H2)],根据可逆反应的特点知a、b、c三者之间的关系是a=b+c;
考点:本题以元素推断为基础,考查原子结构、晶体类型、氢键、元素周期律、元素及化合物、化学平衡常数、热化学方程式的特点等知识。


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:



 或
或
 或
或

 4Al+3O2↑
4Al+3O2↑ 4Al+3O2↑
4Al+3O2↑查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 有关信息 |
| X | 元素主要化合价为-2 |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 与X同主族,其单质在X的单质中燃烧,发出蓝紫色火焰 |
| D | 最高价氧化物既能溶于强酸又能溶于强碱 |
| E | 单质是生活中常见金属,其制品在潮湿的空气中易被腐蚀或损坏 |
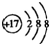
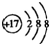
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 信息 |
| X | 位于第三周期,其最高价氧化物水化物的酸性最强 |
| Y | 在第三周期元素中,其第一电离能最小 |
| Z | 单质是生活中常见金属,其制品用量最大,在潮湿空气中易被腐蚀 |
| W | 其基态原子外围电子排布为3S2P1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com