
| ʵ����� | ʵ������ | ������ǿ�� |
| ��ȡһ����FeBr2����ˮ�������������Σ���ˮ����ͨ������������������KSCN��Һ | ��Һ��Ѫ��ɫ | ��Cl2��Fe3+ Br2��Fe3+ |
| ��ȡ����FeBr2����ˮ�����������ˮ����ͨ���������������������Ȼ�̼���� | �����Ȼ�̼����غ�ɫ | Cl2��Br2 |
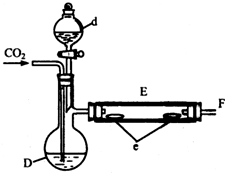
���� ��1������װ��ͼ��֪����d�����ƣ�
��2������ˮ������Ӧ����������������������
A�������к���FeBr3��ȡ�����������Թ��м���ϡ���ᣬ�ټ���KSCN��Һ����Һ��Ѫ��ɫ������˵���������������
B��ȡ����������Ӳ�ʴ��Թ��У�ͨ���������ž���������ȣ���CuSO4�������ɵ�ˮ������˵�������к������������
C��������Ҳ�ܱ��Ż������������������Բ����ܱ�������һ����������������
D��ϸ����Ҳ�Ǻ�ɫ���������ȡ�����������Թ��м�������ˮ�������к�ɫ�����ﲻһ�������������
��3������������Һ�������壬���ɴ������ƺ��廯�ƣ�
��4�����ݵ��ӵ�ʧ�غ��й�ϵʽKMnO4��5Fe2+����Ӧ����ȥKMnO4�����ʵ���Ϊ0.025L��0.03000mol/L=7.5��10-4mol������10g��Ʒ�к���FeBr2�����ʵ���Ϊ7.5��10-4mol��$\frac{250}{25}$��5=0.0375mol���ݴ˿ɼ������Ʒ��FeBr2�Ĵ��ȣ�
��5����֤Cl2��Fe3+��Br2��������ǿ���IJ���Ϊ��ȡһ����FeBr2����ˮ�������������Σ���ˮ����ͨ������������������KSCN��Һ������Һ��Ѫ��ɫ����˵��������Cl2��Fe3+��Br2��Fe3+��ȡ����FeBr2����ˮ�����������ˮ����ͨ���������������������Ȼ�̼���������Ȼ�̼����غ�ɫ����˵��������Cl2��Br2���ݴ˴��⣮
��� �⣺��1������װ��ͼ��֪����d������Ϊ��Һ©����
�ʴ�Ϊ����Һ©����
��2������ˮ������Ӧ�������������������������Ժ���������ΪFe3O4��
A�������к���FeBr3��ȡ�����������Թ��м���ϡ���ᣬ�ټ���KSCN��Һ����Һ��Ѫ��ɫ������˵�����������������A����
B��ȡ����������Ӳ�ʴ��Թ��У�ͨ���������ž���������ȣ���CuSO4�������ɵ�ˮ������˵�������к��������������B��ȷ��
C��������Ҳ�ܱ��Ż������������������Բ����ܱ�������һ������������������C����
D��ϸ����Ҳ�Ǻ�ɫ���������ȡ�����������Թ��м�������ˮ�������к�ɫ�����ﲻһ���������������D����ѡB��
�ʴ�Ϊ��Fe3O4��B��
��3������������Һ�������壬���ɴ������ƺ��廯�ƣ���Ӧ����ʽΪ2NaOH+Br2=NaBr+NaBrO+H2O��
�ʴ�Ϊ��2NaOH+Br2=NaBr+NaBrO+H2O��
��4�����ݵ��ӵ�ʧ�غ��й�ϵʽKMnO4��5Fe2+����Ӧ����ȥKMnO4�����ʵ���Ϊ0.025L��0.03000mol/L=7.5��10-4mol������10g��Ʒ�к���FeBr2�����ʵ���Ϊ7.5��10-4mol��$\frac{250}{25}$��5=0.0375mol��������Ʒ��FeBr2�Ĵ���Ϊ$\frac{0.0375��216}{10}$��100%=81%��
�ʴ�Ϊ��81%��
��5����֤Cl2��Fe3+��Br2��������ǿ���IJ���Ϊ��ȡһ����FeBr2����ˮ�������������Σ���ˮ����ͨ������������������KSCN��Һ������Һ��Ѫ��ɫ����˵��������Cl2��Fe3+��Br2��Fe3+��ȡ����FeBr2����ˮ�����������ˮ����ͨ���������������������Ȼ�̼���������Ȼ�̼����غ�ɫ����˵��������Cl2��Br2��
�ʴ�Ϊ��
| ʵ����� | ʵ������ | ������ǿ�� |
| ��ȡһ����FeBr2����ˮ�������������Σ���ˮ����ͨ������������������KSCN��Һ�� | ��Cl2��Fe3+ Br2��Fe3+ | |
| ��ȡ����FeBr2����ˮ�����������ˮ����ͨ���������������������Ȼ�̼���� | �����Ȼ�̼����غ�ɫ |
���� ���⿼������ȡ�廯����������ƣ��漰�����ݾ�����ѧ��ѧ�еĻ���֪ʶ���������ܣ���ֿ�����ѧ���ķ������������������Ӧ�û�ѧ֪ʶ����������һ�������ϸߵ���Ŀ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ƽ�ⳣ����С | B�� | CaO������ | C�� | ����ѹǿ���� | D�� | CaO2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe��Zn | B�� | Al��Cu | C�� | Al��Na | D�� | Al��Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
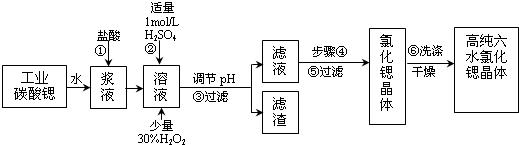
| �������� | Fe��OH��3 | Fe��OH��2 |
| ��ʼ������pH | 1.5 | 6.5 |
| ������ȫ��pH | 3.7 | 9.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ı��˷�Ӧ��;������Ӧ�ġ�HҲ��֮�ı� | |
| B�� | �����¶ȣ��淴Ӧ���ʼӿ죬����Ӧ���ʼ��� | |
| C�� | �����¶ȣ������淴Ӧ���ʶ��ӿ죬��Ӧ�ų����������� | |
| D�� | �ı�ѹǿ��ƽ�ⲻ�����ƶ�����Ӧ�ų����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2S | B�� | BeCl2 | C�� | H3O+ | D�� | NH${\;}_{4}^{+}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܶ� | B�� | ԭ���� | C�� | ���� | D�� | ������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com