
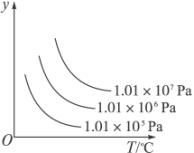
A.平衡混合气体中R的体积分数
B.平衡混合气体中G的体积分数
C.G的转化率
D.L的转化率
 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
 (1)一个确定的化学反应完成后的结果是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小.若反应物的总能量
(1)一个确定的化学反应完成后的结果是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小.若反应物的总能量查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:高中化学 来源:2010年春季武汉睿升学校高一期中考试化学卷 题型:填空题
(9分)⑴一个确定的化学反应完成后的结果是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。若反应物的总能量 (填“>”、“<”、“=”)生成物的总能量,该反应就放出能量;若反应物的总能量 生成物的总能量,该反应就吸收能量。
⑵普通锌锰酸性干电池的内部结构如图所示,请回答
①该电池的负极材料为 该电极反应为
②正极材料为 ,正极得到电子的氧化剂为
③电解质为
⑶化学反应速率通常用单位时间内反应物浓度的减少量或生成物浓度的增加量来表示。若时间用秒表示,则化学反应速率的单位是 。
⑷在外界条件不变的情况下,一个可逆反应达到的最大限度是该反应达到 状态。
查看答案和解析>>
科目:高中化学 来源:2010年春季武汉睿升学校高一期中考试化学卷 题型:填空题
(9分)⑴一个确定的化学反应完成后的结果是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。若反应物的总能量 (填“>”、“<”、“=”)生成物的总能量,该反应就放出能量;若反应物的总能量 生成物的总能量,该反应就吸收能量。
⑵普通锌锰酸性干电池的内部结构如图所示,请回答

①该电池的负极材料为 该电极反应为
②正极材料为 ,正极得到电子的氧化剂为
③电解质为
⑶化学反应速率通常用单位时间内反应物浓度的减少量或生成物浓度的增加量来表示。若时间用秒表示,则化学反应速率的单位是 。
⑷在外界条件不变的情况下,一个可逆反应达到的最大限度是该反应达到 状态。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省成都市双流县棠湖中学外语实验学校高三(上)期中化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com