
 N2(g)+3H2(g),在673K、30MPa下,n(NH3)和n(N2)随时间变化的关系如图所示。下列叙述正确的是
N2(g)+3H2(g),在673K、30MPa下,n(NH3)和n(N2)随时间变化的关系如图所示。下列叙述正确的是 
| A.t1时反应达到平衡 |
| B.t3时,v正(N2)﹥v逆(N2) |
| C.t2时和t3时n(H2)相等 |
| D.t3后,若体积不变充He,反应速率增大 |
科目:高中化学 来源:不详 题型:填空题
 2SO3(g)2 min末测得容器中有7.2 mol SO2。试回答:
2SO3(g)2 min末测得容器中有7.2 mol SO2。试回答: 葡萄糖
葡萄糖 CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动) 甘油和高级脂肪酸
甘油和高级脂肪酸 CO2和H2O(释放能量维持生命活动)
CO2和H2O(释放能量维持生命活动) 氨基酸
氨基酸 人体所需的蛋白质(人体生长发育、新陈代谢)
人体所需的蛋白质(人体生长发育、新陈代谢)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(g)+3H2(g) ΔH>0测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是( )
CO(g)+3H2(g) ΔH>0测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是( )
| A.10 min时,改变的外界条件可能是温度 |
| B.0~5 min内,V(H2)=0.1 mol·L-·min— |
| C.恒温下,缩小容器体积,平衡后c(H2)肯定减小 |
| D.10—12 min时反应的平衡常数逐渐增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(g)+H2(g)△H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
CO(g)+H2(g)△H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。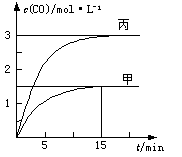
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5 L | 0.5 L | V |
| 温度 | T1 ℃ | T2 ℃ | T1 ℃ |
| 起始量 | 2 molC 1 molH2O | 1 molCO 1 molH2 | 4 molC 2 molH2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g) ?H=—92.4kJ?mol?1
2NH3(g) ?H=—92.4kJ?mol?1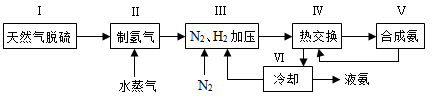
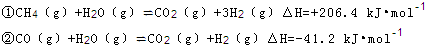
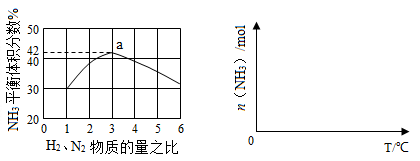
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
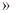
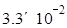 mol/(L·min)
mol/(L·min)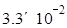 mol/(L·min)
mol/(L·min)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。
bZ(g) △H<0。下图是容器中X、Z的物质的量浓度随时间变化的曲线。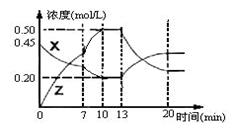
| A.用X表示0~10min内该反应的平均速率为v(X)=0.045mol/(L·min) |
| B.化学方程式中a:b= 1:3, |
| C.推测在第7min时曲线变化的原因可能是增加X的浓度 |
| D.推测该反应处于化学平衡状态的时间是10min--13min及第20min 后 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
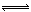 CH3OH(g),根据题意,以下说法正确的是
CH3OH(g),根据题意,以下说法正确的是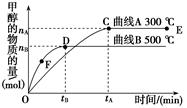
| A.E点的平衡常数大于D点的平衡常数,且该反应的ΔH <0 |
| B.容器中气体的总物质的量E点大于D点 |
| C.当容器内气体密度不变时,说明该反应已达到平衡状态 |
D.v(甲醇)=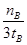 mol/(L·min)-1表示500 ℃以上反应在D点的速率 mol/(L·min)-1表示500 ℃以上反应在D点的速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com