
��֪�����淴ӦN����g��+3H2��g��![]() 2NH3��g����H<0�����мס��������ݻ���ͬ�Ҳ��������ܱ���������������м���1mol N2��g����3mol H2��g������һ�������·�����Ӧ���ﵽƽ��ʱ�ų�����ΪQ1kJ������ͬ�����£����������м���2mol NH3��g����������Ӧ���ﵽƽ��ʱ��������ΪQ2kJ����Q1=3Q2��������������ȷ���ǣ� ��
2NH3��g����H<0�����мס��������ݻ���ͬ�Ҳ��������ܱ���������������м���1mol N2��g����3mol H2��g������һ�������·�����Ӧ���ﵽƽ��ʱ�ų�����ΪQ1kJ������ͬ�����£����������м���2mol NH3��g����������Ӧ���ﵽƽ��ʱ��������ΪQ2kJ����Q1=3Q2��������������ȷ���ǣ� ��
A����ƽ��ʱ����N����ת����Ϊ75��
B����ƽ��ʱ�ס�����NH�������������>��
C���ﵽƽ����������м���0.25mol N2��g����0.75mol H2��g����1.5mol NH3��g����ƽ��������N2�ķ����ƶ�
D�����з�Ӧ���Ȼ�ѧ����ʽΪ2NH3��g��![]() N2��g��+3H2��g����H=+Q2kJ/mol
N2��g��+3H2��g����H=+Q2kJ/mol
 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д� �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 qC��g�����ܱ������н��У���ͼ��ʾ��Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B����������Ĺ�ϵ���ߣ�����ͼ����գ���1������2������3�������������������=������
qC��g�����ܱ������н��У���ͼ��ʾ��Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B����������Ĺ�ϵ���ߣ�����ͼ����գ���1������2������3�������������������=������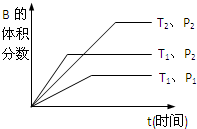
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����4molSO2��2molO2����2L���ܱ������У���һ�������·�����Ӧ����10s��ﵽƽ�⣬���SO3��Ũ��Ϊ0.6mol?L-1����ش��������⣺
��1����4molSO2��2molO2����2L���ܱ������У���һ�������·�����Ӧ����10s��ﵽƽ�⣬���SO3��Ũ��Ϊ0.6mol?L-1����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪ij���淴Ӧ��mA��g��+nB��g��?pC��g����H ���ܱ��������н��У���ͼ��ʾ����Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ�����B%���Ĺ�ϵ���ߣ������߷��������ж���ȷ���ǣ�������
��֪ij���淴Ӧ��mA��g��+nB��g��?pC��g����H ���ܱ��������н��У���ͼ��ʾ����Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ�����B%���Ĺ�ϵ���ߣ������߷��������ж���ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪ij���淴Ӧ��mA��g��+nB��g�� xC��g����H=Q kJ/mol�����ܱ������н�����ͼ��
��֪ij���淴Ӧ��mA��g��+nB��g�� xC��g����H=Q kJ/mol�����ܱ������н�����ͼ���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com