
科目:高中化学 来源: 题型:解答题
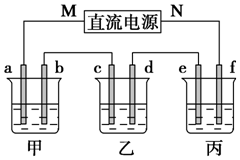 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
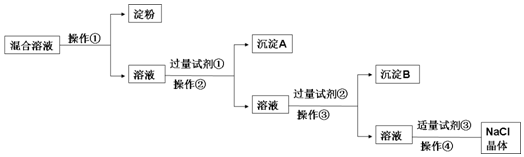
| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
下列变化或过程属于化学变化的是
A.激光法蒸发石墨得C60 B.丁达尔效应
C.紫色石 蕊试液通过活性炭变成无色 D.用铂丝蘸取NaCl溶液进行焰色反应
蕊试液通过活性炭变成无色 D.用铂丝蘸取NaCl溶液进行焰色反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
对于相同物质的量的 SO2与SO3,下列说法正确的是
SO2与SO3,下列说法正确的是
A.硫元素的质量比为5:4 B.原子总数之比为4:3
C.质量之比为1:1 D.分子数之比为1:1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上10月月考化学试卷(解析版) 题型:选择题
科学家 用DNA制造出一种臂长只有7nm的纳米级镊子,这种镊子能钳起分子或原子,并对它们随意组合。下列分散系中分散质的微粒直径与纳米级镊子具有相同数量级的是 ( )
用DNA制造出一种臂长只有7nm的纳米级镊子,这种镊子能钳起分子或原子,并对它们随意组合。下列分散系中分散质的微粒直径与纳米级镊子具有相同数量级的是 ( )
A.溶液 B.胶体 C.悬浊液 D.乳浊液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上第一次学段考试化学卷(解析版) 题型:填空题
为了研究碳酸钙与盐酸反应的反应速率,某同学通过如图实验装置测定反应中生成的CO2气体体积,并绘制出如图所示的曲线。请分析讨论以下问题。


(1)化学反应速率最快的时间段是 ,影响此时间段反应速率的主要因素是 ;
A.O~t1 B.t1~t2 C.t2~t3 D.t3~t4
(2)为了减缓上述反应速率,欲向盐酸中加入下列物质,你认为可行的有 ;
A.蒸馏水 B.NaCl固体 C.NaCl溶液 D.通入HCl
(3)若盐酸的体积是20 mL,图中CO2的体积是标准状况下的体积,则t1~t2时间段平均反应速率v(HCl)= mol·(L·min)-1。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上第一次学段考试化学卷(解析版) 题型:选择题
从海带中提取碘单质,成熟的工艺流程如下:
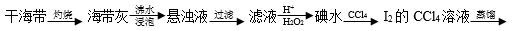
下列关于海水制碘的说法不正确的是
A. 实验室在蒸发皿中灼烧干海带,并且用玻璃棒搅拌
B. 含I-的滤液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C. 在碘水中加入几滴淀粉溶液,溶液变蓝色
D. 碘水加入CCl4得到I2的CCl4溶液,该操作为“萃取”
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com