
(11分)某无色溶液中含有K+、Cl-、OH-、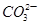 、
、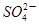 ,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
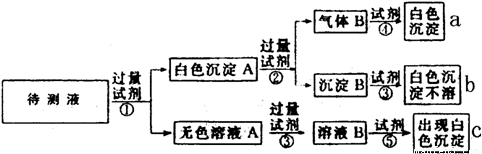
请你根据实验操作及现象分析完成下列各题:
(1)图中现象a、b、c表明检验出的阴离子分别是:
a_________________, b___________________,c_____________________。
(2)白色沉淀A加过量试剂②发生反应的离子方程式是:___________________。
(3)无色溶液A加试剂③的主要目的是:_____________________________________。
(4)白色沉淀A若加试剂③而不加试剂②对实验结果有无影响(选填“有影响”、“无影响"或“无法确定”)____________________________。
(5)气体B通入试剂④中发生反应的离子方程式是:____________________________。
(1)CO32-、SO42-、Cl- (各1分,共3分)
(2)BaCO3+2H+=Ba2++CO2↑+H2O(2分)
(3)中和OH-(或酸化),防止对Cl-的检验产生干扰(2分)
(4)无影响(2分) (5)Ca2++2OH-+CO2=CaCO3↓+H2O(2分)
【解析】本题考查离子推断。由所给试剂的性质特点及反应“气体B+试剂④ 白色沉淀a”,可知试剂④为澄清石灰水,气体B为CO2。又“白色沉淀A+过量试剂②
白色沉淀a”,可知试剂④为澄清石灰水,气体B为CO2。又“白色沉淀A+过量试剂② CO2↑+沉淀B”,则试剂②为盐酸(若试剂②为HNO3则试剂③为盐酸,则会引入Cl-,影响Cl-的检验),且白色沉淀A中含SO42-。又“原无色溶液+过量试剂①
CO2↑+沉淀B”,则试剂②为盐酸(若试剂②为HNO3则试剂③为盐酸,则会引入Cl-,影响Cl-的检验),且白色沉淀A中含SO42-。又“原无色溶液+过量试剂① 白色沉淀A+无色溶液A”,则试剂①为Ba(NO3)2(因AgNO3与OH-作用生成棕黑色Ag2O沉淀),白色沉淀A为BaSO4与BaCO3的混合物,白色沉淀B为BaSO4,试剂③可能为HNO3(联想SO42-的检验方法)。无色溶液A中含Cl-、OH-,经HNO3酸化除去OH-后,所得溶液B中含Cl-,而“溶液B+试剂⑤
白色沉淀A+无色溶液A”,则试剂①为Ba(NO3)2(因AgNO3与OH-作用生成棕黑色Ag2O沉淀),白色沉淀A为BaSO4与BaCO3的混合物,白色沉淀B为BaSO4,试剂③可能为HNO3(联想SO42-的检验方法)。无色溶液A中含Cl-、OH-,经HNO3酸化除去OH-后,所得溶液B中含Cl-,而“溶液B+试剂⑤ 白色沉淀C”,所以试剂⑤为AgNO3,试剂③必为HNO3,C沉淀为AgCl。至此所给试剂和离子全部确定,其他问题便可迎刃而解。
白色沉淀C”,所以试剂⑤为AgNO3,试剂③必为HNO3,C沉淀为AgCl。至此所给试剂和离子全部确定,其他问题便可迎刃而解。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 3 |
| O | 2- 4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
2- 3 |
2- 4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 3 |
| O | 2- 4 |

| A、试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl | ||
| B、现象3中白色沉淀是BaSO4 | ||
C、产生现象2的离子方程式是:Br2+2H2O+SO2=4H++2Br-+S
| ||
| D、试剂②是盐酸,试剂③是硝酸 |
查看答案和解析>>
科目:高中化学 来源:2012届河南省南阳市高三上学期期末质量评估化学试卷(解析版) 题型:填空题
(11分)某无色溶液中含有K+、Cl-、OH-、 、
、 ,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
,为检验确认其中所含的各种阴离子,限用的试剂有:稀盐酸、稀硝酸、硝酸银溶液、硝酸钡溶液、澄清石灰水和酚酞试液,其中检验OH-的实验方法从略,已知检验其他阴离子的过程如下图所示:
请你根据实验操作及现象分析完成下列各题:
(1)图中现象a、b、c表明检验出的阴离子分别是:
a_________________, b___________________,c_____________________。
(2)白色沉淀A加过量试剂②发生反应的离子方程式是:___________________。
(3)无色溶液A加试剂③的主要目的是:_____________________________________。
(4)白色沉淀A若加试剂③而不加试剂②对实验结果有无影响(选填“有影响”、“无影响"或“无法确定”)____________________________。
(5)气体B通入试剂④中发生反应的离子方程式是:____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com