AD
分析:A、常温常压下,气体摩尔体积大于22.4L/mol,所以22.4L混合气体的物质的量小于1mol,结合分子构成判断O个数.
B、铁和过量稀硝酸反应生成铁盐,根据铁和转移电子之间的关系式计算电子个数.
C、碳酸氢根离子能水解导致酸根离子的物质的量小于盐的物质的量.
D、先计算甲烷的物质的量,再根据甲烷和共价键个数的关系式计算共价键个数.
解答:A、常温常压下,气体摩尔体积大于22.4L/mol,所以22.4L混合气体的物质的量小于1mol,虽然每个分子中含有2个氧原子,但22.4L的NO
2和CO
2混合气体含有O 原子小于2 N
A个,故A错误.
B、铁和过量硝酸反应生成铁盐,一个铁原子失去三个电子生成铁离子,所以1 mol Fe 与过量的稀HNO
3反应,转移3 N
A个电子,故B错误.
C、n(NaHCO
3)=0.1mol/L×1L=0.1mol,碳酸氢根离子能水解导致酸根离子的物质的量小于盐的物质的量,所以含有HCO
3-小于0.1N
A个,故C错误.
D、N(CH
4)=n(CH
4)N
A=
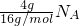
=
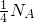
,一个甲烷分子中含有4个共价键,所以4gCH
4含有N
A个C-H共价键,故D正确.
故选D.
点评:本题考查了阿伏伽德罗常数的有关计算,难度不大,注意:有关气体体积的计算都受温度和压强的影响.

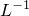 NaHCO3液含有0.1NA个HCO3-
NaHCO3液含有0.1NA个HCO3-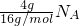 =
=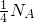 ,一个甲烷分子中含有4个共价键,所以4gCH4含有NA个C-H共价键,故D正确.
,一个甲烷分子中含有4个共价键,所以4gCH4含有NA个C-H共价键,故D正确.

 小学期末标准试卷系列答案
小学期末标准试卷系列答案