
| A.把锌粉改为锌粒 | B.水 | C.Na2CO3固体 | D.降低反应体系温度 |
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源:不详 题型:单选题
 CH3COOCH2CH3+H2O,下列说法错误的是
CH3COOCH2CH3+H2O,下列说法错误的是| A.使用催化剂可以加快反应速率 | B.升高温度可以加快反应速率 |
| C.使用过量乙醇能使乙酸完全转化为乙酸乙酯 | D.该反应属于取代反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O82-)/mol·L-1 | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g)在密闭容器中进行,下列情况中,不能使化学反应速率加快的是
C(g)在密闭容器中进行,下列情况中,不能使化学反应速率加快的是 | A.升高温度 | B.增加A的物质的量 |
| C.使用高效催化剂 | D.将A由块状变成粉末状 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Z(g);△H<0若达到平衡时气体总物质的量变为原来的0.85倍。请回答下列问题。
2Z(g);△H<0若达到平衡时气体总物质的量变为原来的0.85倍。请回答下列问题。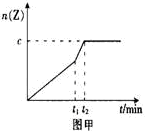
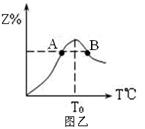
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Z+R的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是()
Z+R的气体反应速率(υ)与时间(t)的关系,t1时开始改变条件,则所改变的条件符合曲线的是() 
| A.减少Z物质 | B.加大压强 | C.升高温度 | D.使用催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.对任何化学反应来说,反应速率越大,反应现象就越明显 |
| B.化学平衡指化学反应的最大限度,改变条件也不能改变化学平衡 |
| C.可逆反应达到化学平衡状态时,正、逆反应的速率都为0 |
| D.升高温度一定能增大反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com