
【题目】设NA为阿伏加德罗常数的值。下列说法错误的是
A. 5NH4NO3![]() 2HNO3+4N2↑+9H2O的反应中,生成28gN2,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O的反应中,生成28gN2,转移的电子数目为3.75NA
B. 常温常压下,7.8gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8NA
C. 若lL0.2mol/L的FeCl3溶液完全水解形成胶体,则胶体粒子数小于0.2NA
D. 标况下22. 4L NO和11.2L O2混合后所得气体分子数为NA
【答案】D
【解析】A.NH4NO3分解反应中,5NH4+中—3价N升高为零价氮,转移5×3=15mole—,5NH4NO3——15mole———4N2,生成28gN2(即1molN2)转移的电子数目为3.75NA,A正确;B.Na2S和Na2O2的摩尔质量相等、阴阳离子个数比相同且阴离子所含电子数相等,故B正确;C. lL0.2mol/L的FeCl3溶液中理论n(Fe3+)=0.2mol,完全水解形成胶体,分子聚集成粒子更大的胶粒,所以胶体粒子数小于0.2NA,故C正确;D. 标况下22. 4L NO和11.2L O2混合后发生:2NO+O2=2NO2反应,NO2再部分二聚,所得气体分子数为小于2NA,故D错误。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最慢的是 ( )
A. 10℃ 20mL 3mol/L的盐酸溶液 B. 10℃ 20mL 1mol/L的盐酸溶液
C. 20℃ 20mL 3mol/L的盐酸溶液 D. 20℃ 20mL 1mol/L的盐酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香柑内酯具有抗菌、抗血吸虫、降血压等作用。它的一种合成路线如下:

(1)C→D的反应类型为_________________。
(2)B的结构简式为_______________________。
(3)E中含氧官能团名称为____________、_______________。
(4)写出同时满足下列条件的D的一种同分异构体的结构简式:____________。
①能发生银镜反应;②能发生水解反应;
③与FeCl3溶液发生显色反应;④分子中只有4种不同化学环境的氢。
(5)己知:![]() 。
。
请以![]() 和CH2=CHCHO为原料制备
和CH2=CHCHO为原料制备![]() ,写出制备的合成路线流程图(常用试剂任用,合成路线流程图示例见本题题干)_______________。
,写出制备的合成路线流程图(常用试剂任用,合成路线流程图示例见本题题干)_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,当关闭K时,向A 中充入2molX、7molY,向B中充入4molX、14molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)![]() Z(g)+2W(g) △H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答:
Z(g)+2W(g) △H<0达到平衡(Ⅰ)时V(B)=0.9a升,试回答:

(1)B中X 的转化率α(X)B为_________________________
(2)A中W和B中Z的物质的量的比较: n(W)A_______________n(Z)B(填<、>、或=)
(3)打开K,过一段时间重新达平衡(Ⅱ)时,B的体积为__________________升 (用含a的代数式表示,连通管中气体体积不计)
(4)要使B容器恢复原来反应前的体积,可采取的措施是_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式及其叙述正确的是( )
A. 氢气的燃烧热为285.5 kJ·mol-1,则电解水的热化学方程式是2H2O(l)=2H2(g)+O2(g) △H=+285.5 kJ·mol-1
B. 1 mol CH4完全燃烧生成CO2和H2O(g)时放出890 kJ热量,其热化学方程式可表示为
![]() CH4(g) +
CH4(g) +![]() O2(g)=2CO2(g)+H2O(g) △H= -445kJ·mol-1
O2(g)=2CO2(g)+H2O(g) △H= -445kJ·mol-1
C. 已知 2C(s) + O2(g)=2CO(g) △H=-221kJ·mol-1 ,则 C 的燃烧热为 221kJ·mol-1
D. 已知NaOH溶液与HCl溶液反应生成1molH2O时放出57.3kJ热量,则NaOH溶液与HF 溶液反应:H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮废水中的氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
![]()
(1)过程Ⅰ:加NaOH溶液,调节pH至11后,并鼓入大量空气。用离子方程式表示加NaOH溶液的作用是______________;用化学平衡理论解释鼓入大置空气的目的__________________。
(2) II中加入适量NaClO溶液,控制pH在3~4,将NH4+转化为无毒物质。则反应的离子方程式是__________________。
(3)分别称取2.39 g (NH4)2SO4和NH4Cl固体混合物两份。
①将其中一份配成溶液,逐滴加入一定浓度的Ba(OH)2溶液,产生的沉淀质量与加入Ba(OH)2溶液体积的关系如图。混合物中n[(NH4)2SO4]:n(NH4Cl)为__________。
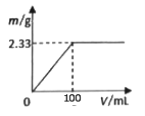
②另一份固体混合物中NH4+与Ba(OH)2溶液(浓度同上)恰好完全反应时,溶液中c(Cl-)=_______ (溶液体积变化忽略不计)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com