
����������ȷ����
A����ӦNH3(g)+HCl(g)  NH4C1(s) ��H<O���κ������¾����Է�����
NH4C1(s) ��H<O���κ������¾����Է�����
B�����ڿ��淴ӦN2(g)+3H2(g)  2NH3(g)��������Ũ�ȿ����ӻ���Ӱٷ������Ӷ�ʹ��Ӧ��������
2NH3(g)��������Ũ�ȿ����ӻ���Ӱٷ������Ӷ�ʹ��Ӧ��������
C����A1C13��Һ��NaAlO2��Һ�ֱ����ɺ����գ����ù�������ΪA1203
D�������ܱ������н��еķ�Ӧ3A(g)  B(g)+c(g)���������������������£��ٳ���һ������A���壬A��ת���ʽ�����
B(g)+c(g)���������������������£��ٳ���һ������A���壬A��ת���ʽ�����
D
��������
���������A����ӦNH3(g)+HCl(g)  NH4C1(s) ��H<O���÷�Ӧ���ؼ�С�ķ�Ӧ���ڵ��������Է����У�����B�����ڿ��淴ӦN2(g)+3H2(g)
NH4C1(s) ��H<O���÷�Ӧ���ؼ�С�ķ�Ӧ���ڵ��������Է����У�����B�����ڿ��淴ӦN2(g)+3H2(g)  2NH3(g)��������Ũ�Ȳ������ӻ���Ӱٷ������������ӻ���������Ӷ�ʹ��Ӧ�������ӣ�����C����A1C13��Һ��NaAlO2��Һ�ֱ����ɺ����գ����ù������ֱ�ΪA1203��NaAlO2������D�������ܱ������н��еķ�Ӧ3A(g)
2NH3(g)��������Ũ�Ȳ������ӻ���Ӱٷ������������ӻ���������Ӷ�ʹ��Ӧ�������ӣ�����C����A1C13��Һ��NaAlO2��Һ�ֱ����ɺ����գ����ù������ֱ�ΪA1203��NaAlO2������D�������ܱ������н��еķ�Ӧ3A(g)  B(g)+c(g)���������������������£��ٳ���һ������A���壬�൱�ڼ�ѹ��ƽ�������ƶ���A��ת���ʽ�������ȷ��ѡD��
B(g)+c(g)���������������������£��ٳ���һ������A���壬�൱�ڼ�ѹ��ƽ�������ƶ���A��ת���ʽ�������ȷ��ѡD��
���㣺���黯ѧ��Ӧ����ѧ��Ӧ���ʵ�Ӱ�����أ��ε�ˮ���Ӧ�ü���ѧ��Ӧ��ת���ʵ�֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡����ۼ��ļ���������ԭ�Ӽ��γ�1mol���ۼ������������̣�ʱ�ͷţ������գ�����������֪H-H ���ļ���Ϊ436kJ��mol-1 ��Cl-Cl���ļ���Ϊ243 kJ��mol-1 ��H-Cl���ļ���Ϊ431 kJ��mol-1 ����H2 (g ) + Cl2 (g ) == 2HCl(g ) �ķ�Ӧ��(��H )����
A��-183 kJ��mol-1 B��183 kJ��mol-1 C��-862 kJ��mol-1 D��862 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ��һ12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и����е�������������ʱ����Ӧ������Ӧ��������ȸı䣬���ɵĻ������ı����
A���������� B�����������������̼
C���������������̼ D������������ˮ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ�߶�12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��ˮ�����ӻ�����KWֻ���¶��йأ�������ᡢ���һ����Ӱ��ˮ�ĵ���̶�
B������HClO��Ka��3.0��10��8��H2CO3��Ka1��4.3��10��7��Ka2��5.6��10��11�����Ʋ���ͬ״���£���Ũ�ȵ�NaClO��Na2CO3��Һ�У�pHǰ�ߴ��ں���
C�������£���0.10 mol��L��1��NH3��H2O��Һ�м�������NH4Cl���壬��ʹ��Һ��pH��С��c(NH4+)/c(NH3��H2O)��ֵ����
D�������£�CH3COOH��Ka��1.7��10��5��NH3��H2O��Kb��1.7��10��5��CH3COOH��Һ�е�c(H��)��NH3��H2O�е�c(OH��)���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ�߶�12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȼ�ϵ�طֱ�ѡ��H2SO4��Һ��NaOH��Һ���������Һ������˵����ȷ����
A���ܷ�Ӧʽ��ΪCH4��2O2===CO2��2H2O
B��H2SO4��NaOH�����ʵ��������䣬��Ũ�ȶ���С
C������H2SO4��Һ���������Һ��������ӦʽΪCH4��4e����H2O===CO2��4H��
D������NaOH��Һ���������Һ��������ӦʽΪO2��2H2O��4e��===4OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У��һ��ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ������
��16�֣���ˮ�к��зdz��ḻ�Ļ�ѧ�ʣ��Ӻ�ˮ�п���ȡ���ֻ���ԭ�ϡ���ͼ��ij�����Ժ�ˮ���ۺ����õ�ʾ��ͼ��
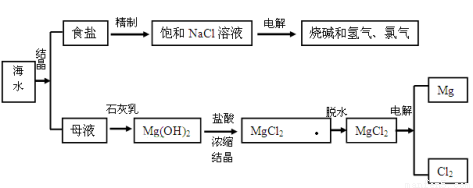
�Իش��������⣺
��1���ҹ������涨ʳ�����б������һ������KIO3������أ������е�Ԫ�صĻ��ϼ�Ϊ �ۡ�
��2��Ϊ��ȥ�����е�Ca2+��Mg2+��SO42-����ɳ�������ǽ���������ˮ��Ȼ�������������������ٹ��ˣ��ڼӹ���������������Һ���ۼ�����������ܼӹ�����̼������Һ���ݼӹ������Ȼ�����Һ�������IJ���˳���� �٢ۣ�����ţ���
��3��д����ⱥ��ʳ��ˮ�Ļ�ѧ����ʽ ����ת��0.2mol����ʱ�������������ɵ��������֮���� ����״���£���
��4���Ժ��߱���Ϊԭ�Ͽ�����ȡʯ���飬���ǵ���Ҫ��ѧ�ɷ�Ϊ ��д��ѧʽ����
��5��Ŀǰ��������������þ��60%�Ժ�ˮ���ɡ�ĸҺ���ơ�þ���Ĺ����У������� �����ֽⷴӦ������Ŀ����
��6������Ȼ�þ���õ����������������������⣬������������ȡƯ�ۣ�Ư�۵���Ч�ɷ�
�� ��д��ѧʽ����
��7������Ҫ��Br����ʽ�����ں�ˮ�У���ȡʳ�κ�ʣ�µ�ĸҺ��Ҳ��±ˮ���У�Br����Ũ�Ƚϴ�ҵ�� �Ʊ���Br2�IJ�������Ϊ��һ�������£���Cl2ͨ��±ˮ�У�����Br2�������ȿ�����Br2������Br2�����ȿ�����������ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У��һ��ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���������ķ�þ���Ͻ��ĩ�ֱ������й�������Һ��ַ�Ӧ���ų�����������
A��NaOH B��ϡH2SO4
C������ D��NaCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�ĵ���У�߶���ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ�з�����ͼͼ�����
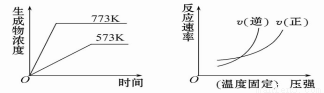
A��N2(g) + 3H2(g)  2NH3(g) ��H =��Q1 kJ��mol-1 (Q1��0)
2NH3(g) ��H =��Q1 kJ��mol-1 (Q1��0)
B��2SO3(g)  2SO2(g) + O2(g) ��H = + Q2 kJ��mol-1 (Q2��0)
2SO2(g) + O2(g) ��H = + Q2 kJ��mol-1 (Q2��0)
C��4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g) ��H =��Q3 kJ��mol-1 (Q3��0)
4NO(g) + 6H2O(g) ��H =��Q3 kJ��mol-1 (Q3��0)
D��H2(g) + CO(g)  C(s) + H2O(g) ��H = + Q4 kJ��mol-1 (Q4��0)
C(s) + H2O(g) ��H = + Q4 kJ��mol-1 (Q4��0)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ����У��һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼΪũ��ɽȪ��Ȫˮƿ�ϵIJ���˵�����֣��г��˸�������Ȼˮ����ָ�ꡣ

����ĸơ�þ���ء�����ָ
A��ԭ�� B��Ԫ�� C������ D������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com