
(10分)某同学用碳棒、纯铜片、直流电源和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu + H2SO4(稀) = CuSO4 + H2↑
(1)请在右边方框中画出能够实现这一反应的装置图。
(2)在设计实验实际操作时,由于装置连接不当,他看到了完全不同的实验现象:碳棒和铜片上均有无色气泡产生,溶液并未变为蓝色。请你分析其原因 ① 。
假设按照该方案进行实验,且收集到碳棒上产生气体体积为11. 2L(标准状况下)。则该过程中铜片上发生的反应式为 ② 。此时要使溶液恢复到实验前的状态,需加入 ③ (写出该物质的化学式),其质量为 ④ 。
(1) 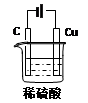
(2)①两极与电源的正负极接反了 ②2H++2e-= H2↑ ③H2O ④18g
解析试题分析:(1)根据方程式可知,Cu做阳极,石墨做阴极,H2SO4做电解质溶液,所以装置图为
(2)如果电极放反,则阳极为:4OH- -4e-=O2↑+2H2O,阴极为2H++2e-=H2↑,所以看不到预期的现象。要想恢复到实验前的状态需要加入水,因为生成O2 11.2L,则需要水18g。
考点:电解池
点评:电解中最关键的是准确判断出电极上离子的放电顺序。在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,所以需要熟练记住常见离子的放电顺序。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 某同学用碳棒、纯铜片、直流电源和稀硫酸为原材料,实现了在通常条件下不能发生的反应:
某同学用碳棒、纯铜片、直流电源和稀硫酸为原材料,实现了在通常条件下不能发生的反应: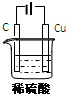

查看答案和解析>>
科目:高中化学 来源:2014届甘肃省高二上学期期末考试化学试卷(解析版) 题型:填空题
(10分)某同学用碳棒、纯铜片、直流电源和稀硫酸为原材料,实现了在通常条件下不能发生的反应:Cu + H2SO4(稀) = CuSO4 + H2↑
(1)请在右边方框中画出能够实现这一反应的装置图。

(2)在设计实验实际操作时,由于装置连接不当,他看到了完全不同的实验现象:碳棒和铜片上均有无色气泡产生,溶液并未变为蓝色。请你分析其原因 ① 。
假设按照该方案进行实验,且收集到碳棒上产生气体体积为11. 2L(标准状况下)。则该过程中铜片上发生的反应式为 ② 。此时要使溶液恢复到实验前的状态,需加入 ③ (写出该物质的化学式),其质量为 ④ 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年甘肃省兰州一中高二(上)期末化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com